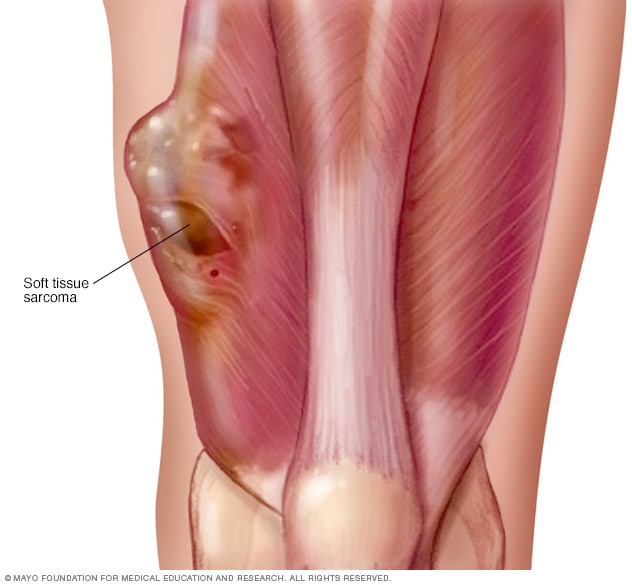
Los avances en el tratamiento de los sarcomas de tejidos blandos son difíciles. Los sarcomas son poco frecuentes y representan menos del 2 % de todos los cánceres. Es difícil realizar estudios a gran escala en poblaciones pequeñas de pacientes, y no es posible demostrar mejoras pequeñas pero significativas en estudios pequeños. La diversidad de este pequeño grupo (hay aproximadamente 70 subtipos de sarcoma y claramente tienen diferentes sensibilidades a los fármacos) explica aún más por qué los oncólogos especializados en sarcomas han hecho pocos avances terapéuticos. La actividad de la doxorrubicina en los sarcomas se descubrió a principios de la década de 1970, cuando no había agentes quimioterapéuticos con eficacia alguna fuera del rabdomiosarcoma pediátrico, y muchos especialistas en sarcomas todavía consideran que la doxorrubicina es el estándar de tratamiento.
La quimioterapia combinada, primero con la adición de dacarbazina y luego con ifosfamida, mejoró las respuestas y la supervivencia libre de progresión, pero nunca se demostró que mejorara la supervivencia general, debido a estudios con poca potencia y a la dilución del efecto beneficioso en algunos subtipos de sarcoma por la inclusión de pacientes en los que no se esperaba ningún beneficio. El sarcoma de tejidos blandos más común, el tumor del estroma gastrointestinal, que es completamente refractario a la quimioterapia estándar, se incluyó en todos los ensayos de sarcomas realizados hasta este siglo, cuando se descubrió su capacidad de respuesta al imatinib, lo que condujo a mejoras notables en la supervivencia.1. Aproximadamente una cuarta parte de los sarcomas de tejidos blandos restantes, los leiomiosarcomas, son en gran medida refractarios a la ifosfamida. No es de extrañar que la combinación de doxorrubicina e ifosfamida en un grupo relativamente pequeño y mixto de sarcomas de tejidos blandos no proporcionara una ventaja en la supervivencia. La trabectedina, introducida a fines de la década de 1990, mostró indicios de eficacia contra los sarcomas de tejidos blandos y fue aprobada para su uso en pacientes previamente tratados en la Unión Europea en 2007. La Administración de Alimentos y Medicamentos (FDA) inicialmente denegó la aprobación debido a la falta de mejora en la supervivencia general que se había observado en el ensayo que condujo a la autorización en la Unión Europea, pero finalmente la FDA dio la aprobación en 2015 para su uso en pacientes con liposarcoma o leiomiosarcoma previamente tratados, esta vez sin considerar la supervivencia. La aprobación anterior en la Unión Europea permitió al Grupo Francés de Sarcomas explorar un mayor uso de este medicamento, mientras que los investigadores estadounidenses se demoraron casi una década con los ensayos de autorización.
Pautier y sus colegas[2] presentan datos a largo plazo sobre la supervivencia sin progresión y la supervivencia general de su elegante ensayo de fase 3 (LMS04)[3], que abordó los dos principales obstáculos para el éxito de ensayos anteriores con pacientes con sarcoma de tejidos blandos: la diversidad y el reducido número de pacientes. Este ensayo se centró en un único subconjunto histológico de sarcomas, el leiomiosarcoma, abordando adecuadamente la conocida diversidad de comportamiento dentro de ese grupo en función del sitio del tumor primario, y se inscribieron suficientes pacientes en el ensayo para detectar una diferencia significativa. Al hacerlo, estos investigadores descubrieron un verdadero beneficio en la supervivencia general, un objetivo que ha eludido a la comunidad del sarcoma durante más de 50 años.
=> Recibir por Whatsapp las noticias destacadas
El presente artículo es la culminación de una serie metódica de estudios realizados por miembros del Grupo Francés de Sarcoma sobre la combinación de doxorrubicina y trabectedina que comenzó hace casi 20 años. Primero, se realizó un estudio formal de fase 1 de la terapia combinada[4], luego un estudio de fase 2 de un solo grupo que incluyó específicamente a pacientes con leiomiosarcoma[5], y luego un ensayo de fase 3 aleatorizado en la misma población. Los investigadores también incorporaron al diseño de su ensayo datos de su estudio de agente único de trabectedina que indicaban mejores resultados con la administración del fármaco a largo plazo[6], así como la práctica común de resecar áreas residuales de enfermedad previamente irresecable o metastásica en pacientes con sarcoma. Lo único que faltaba era un intento de protección cardíaca temprana con doxorrubicina[7] que hubiera permitido la continuación de ambos fármacos o la reinstitución de la terapia con doxorrubicina después de una recaída tardía; sin embargo, tales modificaciones se abordan fácilmente al adoptar este régimen como el nuevo estándar de atención. Finalmente, después de más de 50 años de doxorrubicina como agente único, se ha dado un verdadero paso adelante y ya no se necesita la anticuada quimioterapia con un solo agente. No se puede exagerar la importancia de este ensayo de Pautier y sus colegas, y los investigadores deben ser felicitados.
Por lo tanto, este debería ser un momento de celebración en la comunidad de sarcomas, y deberíamos esperar una serie de ensayos similares en los otros sarcomas en los que la trabectedina ha demostrado actividad, pero lamentablemente, puede ser demasiado tarde. Sin duda, el liposarcoma mixoide, el tumor que es el más sensible a la trabectedina[8,9], sería un objetivo principal para esta terapia combinada, y el liposarcoma desdiferenciado es otro objetivo apropiado para el estudio. Sin embargo, dado el tiempo que tomó llegar a este punto, la U.E. El período de exclusividad de los medicamentos huérfanos ya ha expirado, y la patente estadounidense sobre la trabectedina expirará en 2028. Por lo tanto, ni PharmaMar, el fabricante en España, ni Janssen, la empresa autorizada para vender trabectedina en Estados Unidos, tienen el incentivo financiero para apoyar tales ensayos, ni siquiera para proporcionar el medicamento o modificar la etiqueta de manera que el seguro cubra los costos del medicamento para el desarrollo futuro. Los beneficios superan a la ciencia[sorpresa? No lo creo]. Es de esperar que la modificación de las directrices conduzca a la cobertura del seguro para la trabectedina en pacientes con sarcoma de tejidos blandos no tratados previamente, lo que permitirá una mayor investigación de esta nueva e importante combinación de tratamientos.
Ronald Palacios Castrillo
Referencias bibliográficas
1.
Blanke CD, Rankin C, Demetri GD, et al. Phase III randomized, intergroup trial assessing imatinib mesylate at two dose levels in patients with unresectable or metastatic gastrointestinal stromal tumors expressing the kit receptor tyrosine kinase: S0033. J Clin Oncol 2008;26:626-632.
Go to Citation
2.
Pautier P, Italiano A, Piperno-Neumann S, et al. Doxorubicin–trabectedin with trabectedin maintenance in leiomyosarcoma. N Engl J Med 2024;391:789-799.
Go to Citation
3.
Pautier P, Italiano A, Piperno-Neumann S, et al. Doxorubicin alone versus doxorubicin with trabectedin followed by trabectedin alone as first-line therapy for metastatic or unresectable leiomyosarcoma (LMS-04): a randomised, multicentre, open-label phase 3 trial. Lancet Oncol 2022;23:1044-1054.
Go to Citation
4.
Blay J-Y, von Mehren M, Samuels BL, et al. Phase I combination study of trabectedin and doxorubicin in patients with soft-tissue sarcoma. Clin Cancer Res 2008;14:6656-6662.
Go to Citation
5.
Pautier P, Floquet A, Chevreau C, et al. Trabectedin in combination with doxorubicin for first-line treatment of advanced uterine or soft-tissue leiomyosarcoma (LMS-02): a non-randomised, multicentre, phase 2 trial. Lancet Oncol 2015;16:457-464.
Go to Citation
6.
Le Cesne A, Blay J-Y, Domont J, et al. Interruption versus continuation of trabectedin in patients with soft-tissue sarcoma (T-DIS): a randomised phase 2 trial. Lancet Oncol 2015;16:312-319.
Go to Citation
7.
Benjamin RS, Minotti G. Doxorubicin-dexrazoxane from day 1 for soft-tissue sarcomas: the road to cardioprotection. Clin Cancer Res 2021;27:3809-3811.
Go to Citation
8.
Grosso F, Jones RL, Demetri GD, et al. Efficacy of trabectedin (ecteinascidin-743) in advanced pretreated myxoid liposarcomas: a retrospective study. Lancet Oncol 2007;8:595-602.
Go to Citation
9.
Gronchi A, Palmerini E, Quagliuolo V, et al. Neoadjuvant chemotherapy in high-grade myxoid liposarcoma: results of the expanded cohort of a randomized trial From Italian (ISG), Spanish (GEIS), French (FSG), and Polish Sarcoma Groups (PSG). J Clin Oncol 2024;42:898-906.