Ronald Palacios Castrillo
Aspectos destacados
- La detección de anticuerpos in vitro identificó al CD97 como un antígeno de superficie GSC óptimo
- El CD97 se correlaciona fuertemente con los marcadores intracelulares de GSC
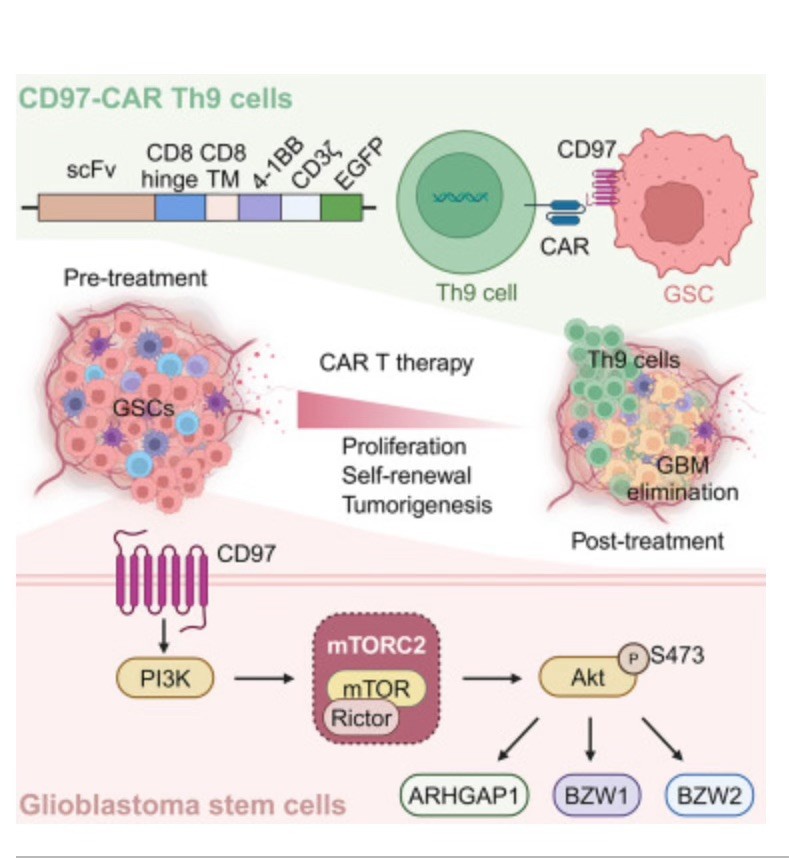
- El CD97 regula la expresión de ARHGAP1, BZW1 y BZW2 a través de la señalización mTORC2-AKT
- Las células CAR Th9 dirigidas al CD97 muestran una potente respuesta antitumoral
Resumen
=> Recibir por Whatsapp las noticias destacadas
Las células madre del glioblastoma (GBM) contribuyen a un mal pronóstico en pacientes con GBM. La identificación de marcadores moleculares es crucial para desarrollar terapias dirigidas. Zhou,et.al.,[Cell Reports Medicine, DOI: 10.1016/j.xcrm.2024.101844] identificaron el grupo de diferenciación 97 (CD97) como un antígeno de superficie GSC óptimo para la posible focalización mediante terapia de células T con receptor de antígeno quimérico (CAR) a través de la detección de anticuerpos in vitro.
El CD97 se expresa de manera consistente en todas las GSC derivadas de pacientes validadas y se correlaciona positivamente con los marcadores intracelulares de GSC conocidos.
El silenciamiento del CD97 reduce las actividades relacionadas con la tumorigenicidad de las GSC, incluida la autorrenovación, la proliferación y la progresión tumoral.
El análisis del transcriptoma revela que CD97 activa mTORC2, lo que conduce a la fosforilación de AKT S473 y a una mayor expresión de los genes dependientes ARHGAP1, BZW1 y BZW2. La inhibición de mTORC2 con JR-AB2-011 suprime la tumorigenicidad de las GSC y la expresión de genes dependientes.
Los autores desarrollaron células T auxiliares (Th) 9 CD97-CAR, que exhiben potentes efectos citotóxicos in vitro y prolongan la supervivencia en ratones.
Estos hallazgos sugieren que CD97 es un antígeno prometedor enriquecido con GSC y que dirigirlo con células CAR Th9 ofrece una posible estrategia terapéutica para el GBM.