Resumen
La dexametasona es un tratamiento que salva vidas para la COVID-19 grave, pero se desconoce su mecanismo de acción y muchos pacientes se deterioran o mueren a pesar del inicio oportuno del tratamiento. Knoll y colaboradores (CELL,2024. DOI:https://doi.org/10.1016/j.cell.2024.06.014), identificaron cambios celulares y moleculares inducidos por el tratamiento con dexametasona asociados con una mejor supervivencia en pacientes con COVID-19 grave. Observaron una reversión de las firmas transcripcionales distintivas en monocitos asociadas con COVID-19 grave y la inducción de un subestado de monocitos caracterizado por la expresión de genes de respuesta a corticosteroid es. Estas respuestas moleculares a la dexametasona se detectaron en monocitos circulantes y pulmonares y se relacionaron directamente con la supervivencia. Las firmas derivadas de la secuenciación de RNA unicelular de monocitos (scRNA-seq) se enriquecieron en transcriptomas de sangre completa de pacientes con desenlace fatal en dos cohortes independientes, lo que destaca el potencial para identificar a los que no responden y son refractarios a la dexametasona. Los hallazgos de Knoll y colegas vinculan los efectos de la dexametasona con la inmunomodulación específica y la reversión de la desregulación de los monocitos, y resaltan el potencial de las ómicas unicelulares para monitorear la participación objetivo in vivo de fármacos inmunomoduladores y para la estratificación de pacientes para enfoques de medicina de precisión.
En Detalle
=> Recibir por Whatsapp las noticias destacadas
Los GC se encuentran entre los fármacos más recetados en todo el mundo y son una piedra angular para el tratamiento de una variedad de afecciones inflamatorias agudas y crónicas. En la práctica clínica, a menudo se los considera inmunosupresores eficaces aunque bastante inespecíficos, a pesar del conocimiento molecular establecido de que tanto los GC naturales como los diseñados farmacológicamente actúan mediante unión específica a los receptores de GC. Se sabe que la capacidad de respuesta al tratamiento con GC es heterogénea entre los pacientes ,posiblemente influenciado por la variedad de diversas isoformas del receptor de GC, que median sus efectos diferenciales genómicos y no genómicos.
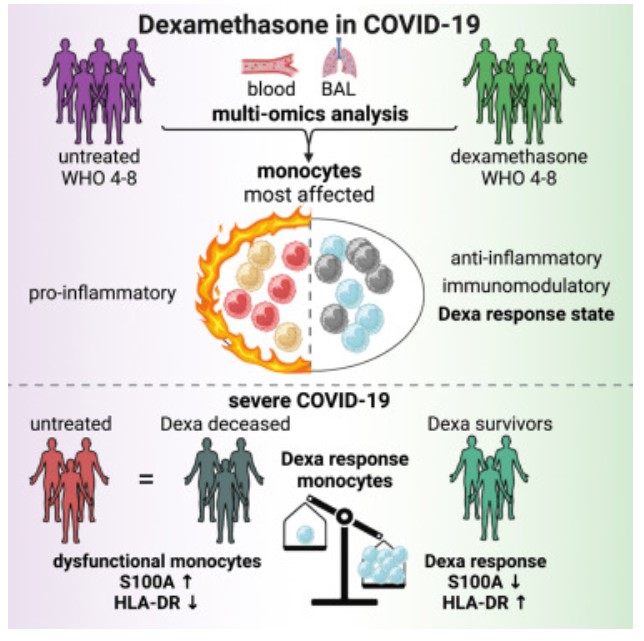
Para comprender mejor la especificidad y el modo de acción molecular del tratamiento con GC en COVID-19, Knoll y colegas aplicaron transcriptómica masiva de alto contenido y tecnologías unicelulares de alta resolución en dos cohortes clínicas de pacientes con COVID-19. Proporcionan evidencia de que el tratamiento con dexametasona en casos graves de COVID-19 conduce a una modulación inmune altamente específica. Los cambios importantes de los fenotipos moleculares ocurren principalmente en el compartimento de las células mieloides( neutrófilos,monocitos,macrófagos), donde la dexametasona provoca un estado celular específico del tratamiento en una fracción de monocitos, con la inducción de genes con funciones reguladoras bien conocidas, incluidos receptores de la superficie celular, reguladores transcripcionales y reguladores traduccionales, mientras que muchas quimiocinas e IL-1B tienen una expresión disminuida. La definición de los efectos cualitativos y cuantitativos del tratamiento con dexametasona a nivel celular y molecular respaldó un efecto inmunomodulador específico, con muchos cambios inducidos independientemente de la gravedad de la enfermedad. Es importante destacar que estos efectos recuerdan los cambios descritos previamente en otros entornos terapéuticos, como la artritis reumatoide, las enfermedades inflamatorias intestinales o el asma alérgica, por ejemplo, el aumento de la expresión de ciertos genes con función reguladora, incluida la trombospondina 1 (THBS1), IL1R2, o la proteína cremallera de leucina GILZ (TSC22D3) inducida por GC. El enriquecimiento funcional entre tipos de células apunta a una fuerte interferencia con la señalización de NF-κB, que es uno de los mecanismos bien conocidos posteriores a la señalización del receptor de GC.
Lo más sorprendente es que la respuesta molecular a la dexametasona se vinculó con la respuesta y el resultado del tratamiento clínico, ya que el fenotipo molecular disfuncional previamente descrito asociado con la COVID-19 aguda grave (monocitos HLA-DRloS100Ahi) se revirtió en pacientes que sobrevivieron a la COVID-19 grave. Esto ilustra que la terapia con dexametasona en esta situación clínica no sólo es inmunosupresora sino también inmunomoduladora, ya que se restableció la expresión de genes relacionados con una función inmune eficaz. De hecho, un estado de respuesta Dexametasona específico dentro de los monocitos, descubierto mediante el análisis del transcriptoma unicelular, reveló que no todos los monocitos responden al tratamiento. Los pacientes que sucumbieron a la enfermedad no mostraron una reversión del fenotipo molecular disfuncional en el compartimento de los monocitos (monocitos HLA-DRloS100Ahi), acompañado por una falta del estado de las células de los monocitos en respuesta a la dexametasona en la mayoría de estos pacientes.
La firma de respuesta a la dexametasona de los monocitos sanguíneos también se enriqueció en monocitos y macrófagos de muestras de BAL(lavado broncoalveolar de pulmón) de sobrevivientes tratados con dexametasona, pero no de los no sobrevivientes tratados o de pacientes sin tratamiento previo con GC de la cohorte. El papel de los monocitos inflamatorios y potencialmente profibróticos y de los macrófagos derivados de monocitos en el desarrollo del síndrome de dificultad respiratoria aguda (SDRA) en la COVID-19 se ha documentado en numerosos estudios. La reversión del fenotipo molecular disfuncional de los monocitos en el pulmón, asociado con el tratamiento con dexametasona y un resultado positivo (supervivencia), vincula estos hallazgos en las células inmunes circulantes con la protección inducida por el tratamiento con dexametasona.
Las diferencias en los cambios transcripcionales después del tratamiento estuvieron precedidas por cambios epigenéticos en el programa proinflamatorio de los monocitos CD14+, que también difirieron entre los que respondieron y los que no respondieron. Una firma relacionada con los resultados generada a partir de los transcriptomas de monocitos (8 días después del inicio del tratamiento) se aplicó con éxito a transcriptomas de sangre completa muestreados incluso antes, dentro de dos cohortes observacionales más grandes de un solo centro y multicéntrico, respectivamente. La firma se enriqueció en transcriptomas de sangre total de pacientes que sucumbieron a la COVID-19 en este estudio de un solo centro ya 4 días después del inicio del tratamiento, lo que indica un fracaso temprano del tratamiento. Las pruebas de generalización de este posible predictor de la respuesta y el resultado del tratamiento en una cohorte multicéntrica nacional en un momento incluso anterior revelaron que se requieren más de dos días de tratamiento para la estratificación del resultado molecular.
Se han realizado varios intentos para identificar subgrupos de pacientes con COVID-19 grave que probablemente respondan de manera diferente al tratamiento antiinflamatorio. Se informó que dos grupos distintos de pacientes con SDRA relacionado con COVID, similares a los subfenotipos de SDRA hipoinflamatorio e hiperinflamatorio descritos anteriormente, mostraron una respuesta diferencial al tratamiento con corticosteroides y se propusieron una dosificación de corticosteroides guiada por biomarcadores en COVID-19. De manera similar, se han utilizado transcriptomas de sangre periférica para identificar dos endotipos diferentes de pacientes con COVID-19 grave según genes relacionados con IFN o de puntos de control, que mostraron efectos específicos de grupo del tratamiento con corticosteroides. Los intentos de identificar diferentes endotipos o fenotipos de COVID-19 en términos de su respuesta al tratamiento antiinflamatorio son particularmente importantes a la luz del hecho de que varios ensayos clínicos inicialmente no lograron demostrar un beneficio claro en la supervivencia del tratamiento con corticosteroides en COVID-19, en además del hecho de que sólo alrededor de un tercio de los pacientes con COVID-19 grave con ventilación mecánica se benefician de la terapia con dexametasona. Existe una larga historia de trabajos que investigan la capacidad de respuesta de los GC, basada en la conocida heterogeneidad en la respuesta al tratamiento y la variedad de efectos desfavorables de los corticosteroides, particularmente asociados con su uso a largo plazo. En el asma, se han definido distintos endotipos en función del nivel de inflamación tipo 2, que se sabe que predice la respuesta al tratamiento con GC. Además, en otras afecciones clínicas, por ejemplo, la neumonía adquirida en la comunidad, la importancia del tratamiento con esteroides no es totalmente evidente, con signos claros de que ciertos grupos de pacientes se benefician más del tratamiento complementario con corticosteroides que otros, lo que enfatiza la importancia de la estratificación temprana de los pacientes. En mi opinión, el enfoque presentado en este estudio va un paso más allá de la estratificación molecular y la definición de endotipos de enfermedades al proporcionar información directa sobre la respuesta a la terapia como una forma de seguimiento de la terapia molecular. El potencial de las firmas basadas en transcriptomas de sangre total para optimizar los regímenes de tratamiento con dexametasona debe evaluarse en un ensayo fundamental prospectivo en el futuro.
Limitaciones del estudio
El análisis de los efectos del tratamiento con dexametasona se basó en un gran estudio de cohorte prospectivo de un solo centro y un estudio de cohorte prospectivo multicéntrico independiente para la validación del enriquecimiento de la firma transcripcional asociado con un desenlace fatal. Una limitación importante de este enfoque es el hecho de que ambas cohortes fueron observacionales y no fueron diseñadas principalmente para estudiar el efecto del tratamiento con dexametasona. Sin embargo, se aprovechó el hecho de que el tratamiento con dexametasona solo se introdujo en el SOC en la segunda ola, lo que permitió una comparación bien ajustada de pacientes con COVID-19 con demografía y gravedad de enfermedad similares, infectados con la misma variante viral (D614G) , que difería sólo por el tratamiento. No obstante, sería preferible realizar estudios de esta naturaleza en el marco de ensayos controlados aleatorios, diseñados para estudiar los criterios de valoración clínicos, así como los mecanismos de acción de los fármacos investigados. Por lo tanto, los ensayos de plataformas adaptativas, como el estudio RECOVERY, diseñado para probar rápidamente la eficacia de medicamentos reutilizados o nuevas terapias en emergencias de salud pública, se beneficiarían de la incorporación de estudios de biomarcadores de alta resolución para descubrir mecanismos e identificar poblaciones objetivo y de riesgo que beneficiarse más del respectivo tratamiento o terapias alternativas. Con este fin, se necesitan redes globales de instituciones médicas especializadas capaces de aplicar métodos altamente estandarizados y de alta resolución en muestras de estudio con un alto rendimiento para facilitar este desarrollo acelerado de tratamientos. Si bien el enfoque incluyó cohortes bien emparejadas, el período de estudio se limitó a la fase inicial de la pandemia. Esta es una limitación ya que las características inmunológicas y virológicas han cambiado durante el transcurso de la pandemia. La dexametasona sigue siendo el SOC para pacientes con COVID-19 de moderada a grave; sin embargo, se desconoce si sigue siendo igualmente eficaz en infecciones recurrentes e irruptivas. El uso de corticosteroides en otras infecciones respiratorias ha sido controvertido, con efectos potencialmente perjudiciales en las infecciones por influenza y resultados mixtos en la neumonía adquirida en la comunidad. Sin embargo, será difícil generar nuevos datos ya que no sería ético suspender la dexametasona en pacientes con COVID-19 grave.
Este estudio tiene varias implicaciones. En primer lugar, el tratamiento con corticosteroides(GC) en la COVID-19 aguda se caracteriza mejor como una terapia inmunomoduladora que como inmunosupresora. En segundo lugar, los predictores tempranos de resultados podrían guiar la terapia personalizada al identificar a los pacientes que no responden adecuadamente a los GC, lo que requiere la adición temprana de otros inmunomoduladores como los inhibidores de la Janus quinasa o los bloqueadores del receptor de IL-6. Como se ha informado que la terapia con GC en dosis altas aumenta la mortalidad en pacientes hipóxicos de moderados a graves que no requieren ventilación mecánica, el tratamiento prolongado con dexametasona en pacientes graves con COVID-19 también podría aumentar el riesgo de infecciones secundarias y, por lo tanto, podría contribuir a reducir las tasas de supervivencia en este subgrupo de pacientes. En tercer lugar, sería muy deseable un uso más preciso de los GC en otras afecciones médicas, y se podría lograr una estratificación más precisa basada en ensayos clínicos que incorporen estudios de biomarcadores de resolución unicelular.
En conjunto, los investigadores proporcionan información de fenotipo molecular resuelto a nivel de una sola célula para el efecto inmunomodulador del tratamiento con dexametasona en pacientes con COVID-19 grave, que podría utilizarse para la toma de decisiones clínicas con respecto a la reevaluación de la terapia para el tratamiento con dexametasona en el futuro. Combinado con enfoques de predicción inversa de objetivos de fármacos basados en transcriptomas y ensayos controlados aleatorios, este enfoque puede formar la base para soluciones más rápidas de reutilización de fármacos para futuras enfermedades infecciosas emergentes, e incluso puede ser un modelo para el desarrollo de medicina de precisión para otras enfermedades infecciosas y no infecciosas. -enfermedades infecciosas.
El beneficio de la dexametasona para salvar vidas en casos graves de COVID-19 está relacionado con una reversión de la desregulación de los monocitos