Creo que es una ocasión excelente para actualizar los mecanismos que conducen a que una persona padezca SLE.
Primero, a continuación resumo el reciente trabajo de Mori y sus colaboradores quienes demostraron el mecanismo por el cuál se pueden generar linfocitos T autoreactivos en pacientes con SLE.[ Mori,et.al.,CELL.DOI: 10.1016/j.cell.2024.08.025].
Aspectos destacados
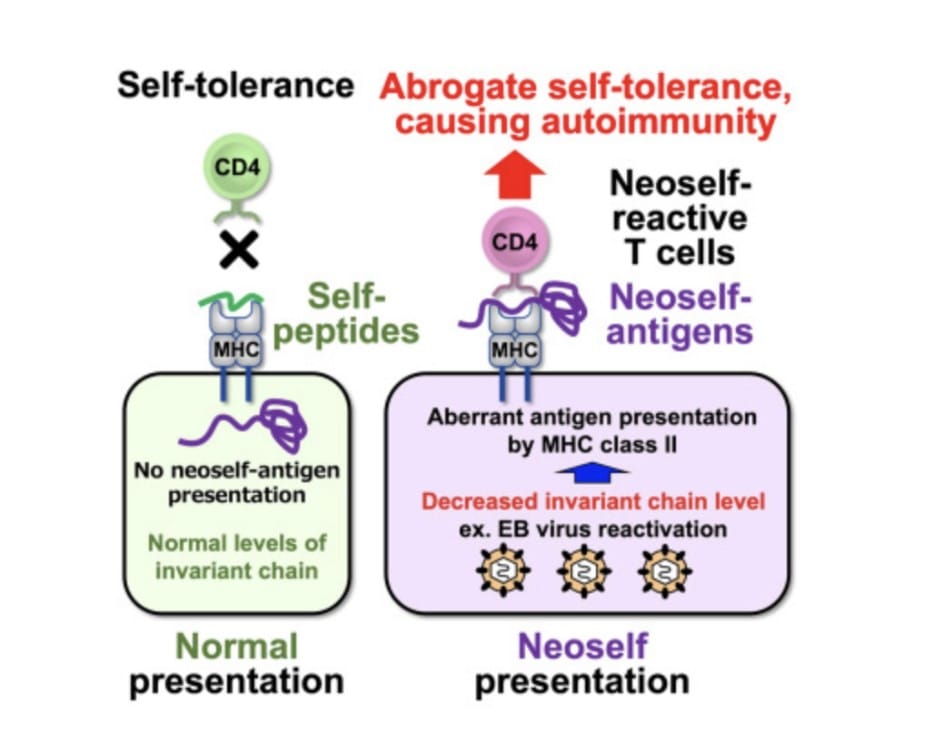
Los neoautoantígenos se presentan en el MHC-II Cuando hay niveles bajos de la cadena invariante
=> Recibir por Whatsapp las noticias destacadas
La enfermedad similar al lupus se desarrolló tras la eliminación de la cadena invariante de ratones adultos
Se encontró expansión clonal de células T neoautoreactivas en pacientes con LES
La reactivación del virus de Epstein-Barr es uno de los factores que promueven la presentación de neoautoantígenos
Resumen
El complejo mayor de histocompatibilidad de clase II (MHC-II) es el factor de riesgo genético más significativo para el lupus eritematoso sistémico (SLE), pero la naturaleza de los autoantígenos que desencadenan la autoinmunidad sigue sin estar clara. Los autoantígenos inusuales, denominados neoautoantígenos, se presentan en MHC-II en ausencia de la cadena invariante esencial para la presentación normal de péptidos. Aquí, Mori,et.al.,[CELL.DOI: 10.1016/j.cell.2024.08.025] demostraron que los neoautoantígenos son el objetivo principal de las células T autorreactivas expandidas clonalmente en el SLE. Cuando se indujo la presentación de neoautoantígenos eliminando la cadena invariante en ratones adultos, las células T neoautoreactivas se expandieron clonalmente, lo que llevó al desarrollo de una enfermedad similar al lupus. Además, descubrieron que las células T CD4+ neoautoreactivas se expandieron significativamente en pacientes con SLE. Una alta frecuencia de reactivación del virus de Epstein-Barr es un factor de riesgo para el SLE. Las células T lúpicas neoautoreactivas fueron activadas por células reactivadas por el virus de Epstein-Barr a través de la regulación negativa de la cadena invariante. En conjunto, los hallazgos implican que la presentación de antígenos neoautoreactivos por MHC-II desempeña un papel crucial en la patogénesis del SLE. Estos hallazgos completan el proceso por el cuál una persona padece SLE (ver abajo).
En lo que sigue trataré de resumir el proceso a través del cuál una persona llega a padecer SLE.
En el SLE hay factores genéticos predisponentes y factores ambientales que desencadenan o activan la enfermedad.Entre los factores genéticos están:a) los genes defectuosos AIRE esenciales en la tolerancia a proteínas propias que aprenden en el timo los linfocitos T durante su diferenciación antes de emigrar a la periferia; b) los genes para el reconocimiento de las células en proceso de morir(apoptosis) , para la captación y destrucción de las células muertas dentro de los macròfagos( encargados de eliminar las células en vías de o muertas en el organismo, genes que afectan los sensores intracelulares en las células presentadoras de antìgenos (cels. Dendrìticas,macròfagos) que detectan la presencia de DNA nativo y RNA;c) genes que regulan la producción de interferon alfa(tipo I) y la expresión de genes del sistema de histocompatibilidad(HLA) clase II asociado con la presentación de neoautoantígenos HLA-DR3/4 (el trabajo citado arriba).
Normalmente, las miles de células que mueren diariamente en nuestro organismo en su mayorìa por apoptosis son reconocidas por los macrófagos que detectan a las células en proceso de morir o ya muertas, las ingieren y metabolizan para la reutilizaciòn de proteínas o desintegración y eliminación del organismo. Imaginen que los macrófagos son los que recolectan la basura, la cargan en volquetas y las desechan en vertederos asignados. Pues bien, los pacientes con SLE tienen falla en el sistema recolector de basura.Como una gran parte del material de las células muertas(la basura) lo constituye el DNA y el RNA de los núcleos, esto se acumula hasta alcanzar niveles que pueden estimular la respuesta innata y adaptativa del sistema inmunológico. Hay pacientes con SLE en quienes sus sensores intracelulares para DNA(TLR9) o RNA(TLR 7/8) son hiperactivos e hipersensibles y estimulan fuertes respuestas inmunológicas contra los neoantígenos(DNAds, varios tipos de RNA). De ahí que los pacientes con SLE casi siempre tienen auto anticuerpos contra ácidos nucleares(ANA), DNA nativo y RNA de varios tipos Ej. SSA,SSB. Estos autoanticuerpos se usan para el diagnóstico de los pacientes con SLE. La hiper respuesta inmuno-inflamatoria es responsable del daño de los òrganos y tejidos.
Entre los factores desencadenantes o activadores del SLE están; A) los rayos ultravioleta cómo el sol(esto mata a las células de la piel y se produce mucha más basura, es decir DNA/RNA que estimulan al sistema inmune; B)el SLE es mucho más frecuente en la mujer y se debe a 2 factores:1)la mujer tiene 2 cromosomas X , en el cromosoma X se encuentran los genes que codifican los sensores intracelulares para RNA [TLR7/8] y DNA[TLR9] por lo tanto la mujer tiene doble sensitividad al DNA/RNA intracelulares en las células dendríticas y macrófagos y 2) los estrógenos favorecen la producción de autoanticuerpos por los linfocitos B y la producción de Interferon tipo I que participa en el proceso inmuno-inflamatorio del SLE.
- C) Las infecciones al causar inflamación y muerte celular pueden activar al SLE. Caso especial es la infección/reactivaciòn de los virus citomegalovirus y Epstein Barr(EBV) .El EBV directamente activa a los linfocitos B a producir anticuerpos incluyendo los que producen autoanticuerpos contra DNA/RNA desencadenando asì activación del SLE. El trabajo de Mori y colegas ańade una pieza importante en la patogénesis del SLE[ Mori,et.al.,CELL.DOI: 1016/j.cell.2024.08.025], resumido arriba, indica que el EBV inhibe la síntesis de la cadena Invariante en el retículo endoplasma intracelular, favoreciendo la presentación de auto/neo antìgenos provenientes de proteínas mal ensambladas. Esto, cómo demuestran Mori y colegas, activa linfocitos T y B autoreactivos contra DNA/RNA en personas genéticamente susceptibles a padecer SLE. Normalmente la cadena invariante está pegada al HLD-DR en el reticuloendoplasma hasta que se encuentra con peptidos de proteínas bien ensambladas proveniente de patógenos que al unirse al bolsillo especial de HLA-DR resulta en la liberación de la cadena intermedia y luego se expresan los complejo antìgeno/HLA-DR en la membrana celular para que activen a linfocitos T y B especìficos para el antìgeno en cuestión.
Dado que todas las células del organismo humano(un trillón de células aproximadamente) excepto los glóbulos rojos, tienen núcleos que contienen DNA/RNA y por lo tanto, son susceptibles de ser atacadas por los linfocitos T autoreactivos y los autoanticuerpos contra DNA/RNA, esto explica porqué el SLE puede afectar cualquier órgano y tejido del organismo, es decir es una enfermedad sistémica. Por otro lado, el hecho de que cada persona con SLE tiene un único patrón de los genes defectuosos que causan esta enfermedad(cómo se resumió arriba) hace que cada paciente presente un cuadro clínico y comportamiento de la enfermedad de manera única,esto es, cada paciente con SLE es ÙNICO y debe ser tratado individualmente!
Ronald Palacios Castrillo,M.D.,PhD.