Aspectos destacados
El mRNA de IDO1 humano que contiene un ancla de membrana intracelular aumenta el nivel de proteína
La administración de mRNA de IDO1 anclado reduce la gravedad de la enfermedad en EAE, CIA y aGVHD
Expresión hepática de IDO1 anclado es necesaria para la protección en modelos autoinmunes
=> Recibir por Whatsapp las noticias destacadas
La eficacia de IDO1 administrada mediante mRNA se asocia con niveles reducidos de triptófano sérico
Resumen
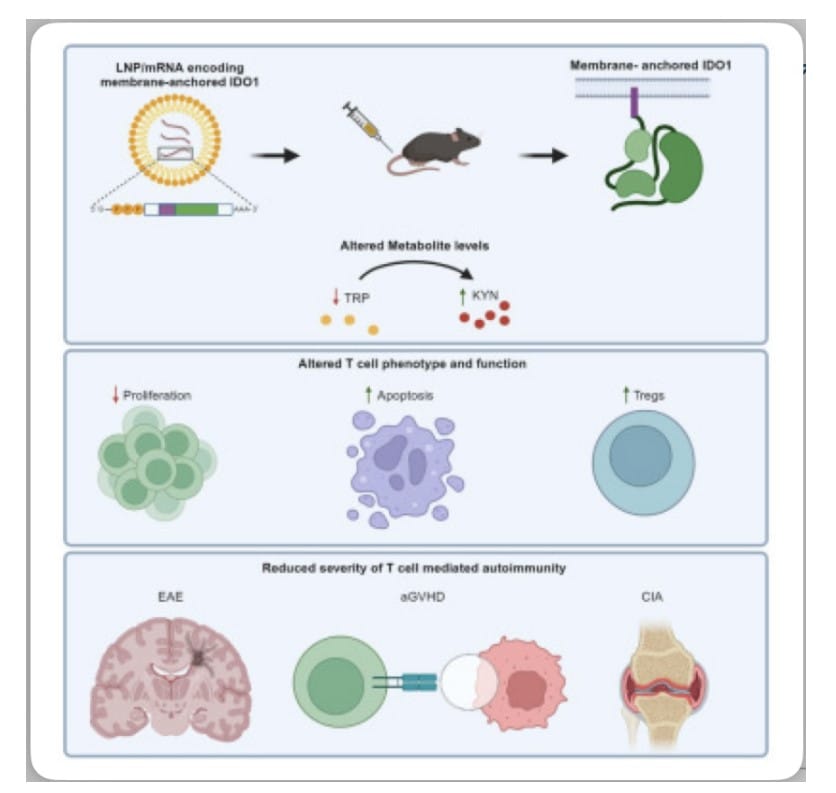
La indolamina-2,3-dioxigenasa (IDO)1 degrada el triptófano, obtenido a través de la ingesta dietética, en metabolitos inmunorreguladores de la vía de la quinurenina. La deficiencia o el bloqueo de IDO1 da como resultado la mejora de la gravedad autoinmune en modelos de roedores y una mayor susceptibilidad a desarrollar autoinmunidad en humanos. A pesar de esto, las modalidades terapéuticas que aprovechan IDO1 para el tratamiento de la autoinmunidad siguen siendo limitadas. Kenney,et.al., [Cell Reports Medicine.DOI: 10.1016/j.xcrm.2024.101717] utilizaron RNA mensajero (m) formulado en nanopartículas lipídicas (LNP) para administrar una variante humana de IDO1 que contiene el sitio de miristoilación de Src para anclar la proteína a la cara interna de la membrana plasmática. Esta IDO1 anclada a la membrana ha aumentado la producción de proteínas, lo que conduce a mayores cambios en los metabolitos y, en última instancia, mejora la enfermedad en tres modelos de autoinmunidad mediada por células T: encefalomielitis autoinmune experimental (EAE), artritis inducida por colágeno en ratas (CIA) y enfermedad de injerto contra huésped aguda (aGVHD). La eficacia de IDO1 se correlaciona con la expresión hepática y el agotamiento sistémico del triptófano. Por lo tanto, la administración de IDO1 anclada a la membrana por mRNA suprime la respuesta inmunitaria en varios modelos bien caracterizados de autoinmunidad.