(i.e.semaglutida,tirzepatida)
Ronald Palacios Castrillo,M.D.,PhD.
=> Recibir por Whatsapp las noticias destacadas
Resumen
Los agonistas del receptor del péptido similar al glucagón-1 (GLP-1) son análogos de incretinas que favorecen la secreción de insulina mediada por glucosa y se emplean en el tratamiento de la diabetes mellitus tipo 2 y la obesidad. Los agonistas del receptor GLP-1, así como los agonistas duales de GLP-1 y del péptido insulinotrópico dependiente de glucosa (GIP), operan a través de múltiples mecanismos: reducción del vaciamiento gástrico, inhibición de la secreción de glucagón, modificaciones beneficiosas en el microbioma intestinal y efectos directos sobre los núcleos hipotalámicos que potencian la saciedad y, con ello, la pérdida de peso. Más allá de sus notables efectos sobre la glucemia y el peso corporal, ensayos aleatorizados y controlados de gran envergadura han demostrado que estos agonistas reducen el riesgo cardiovascular y ralentizan la progresión hacia la insuficiencia renal tanto en individuos de alto riesgo como en aquellos con diabetes tipo 2. Sus efectos adversos son predominantemente gastrointestinales, aunque también pueden incluir pérdida de masa muscular y ósea. Subsisten interrogantes sobre la adherencia a largo plazo, el rebote ponderal tras la interrupción del tratamiento y las repercusiones funcionales de la pérdida de masa magra y ósea. Estudios dirigidos recientes y en curso apuntan a posibles indicaciones adicionales para los agonistas del receptor GLP-1.
En la actualidad, más de mil millones de personas en el mundo padecen obesidad, y muchas de ellas presentan asimismo diabetes mellitus tipo 2 o prediabetes.¹ La irrupción reciente de terapias innovadoras que inducen pérdida de peso y mejoran el control glucémico ha despertado esperanza y expectativas de que estas patologías puedan controlarse de forma efectiva. No obstante, el advenimiento de estos nuevos agentes plantea el dilema clínico de cómo emplearlos de manera segura y costo-efectiva.² La presente revisión describe una nueva generación de tratamientos para personas con obesidad, con o sin diabetes o prediabetes.
Descubrimiento y desarrollo farmacológico
El descubrimiento de los péptidos insulinotrópicos discurre en paralelo con los orígenes de la historia de la insulina. A finales del siglo XIX, los experimentos en modelos animales revelaron que la ablación pancreática inducía hiperglucemia, caquexia y, en última instancia, la muerte. Transcurrieron treinta años hasta que Banting y Best aislaran y purificaran la insulina y la aplicaran con éxito en el tratamiento de un paciente diabético.³ Poco después, un equipo británico identificó moléculas intestinales capaces de reducir la glucemia y las denominó incretinas.⁴ Posteriormente, la extraordinaria eficacia de la insulina en el control de la hiperglucemia eclipsó la investigación sobre las incretinas hasta que trabajos seminales de Habener, Drucker, Holst, Bloom y otros demostraron que estas constituían moléculas insulinotrópicas potentes.⁵⁻¹² En su conjunto, tales estudios identificaron y caracterizaron el péptido similar al glucagón-1 (GLP-1) en las células L intestinales como un producto peptídico derivado del glucagón (aminoácidos 7 a 37). En 1990, John Eng aisló del veneno del lagarto monstruo de Gila la exendina-4, péptido nativo estructuralmente afín al GLP-1, que compite por su receptor, estimula la secreción de insulina y exhibe una vida media más prolongada.¹²⁻¹⁴ Los efectos hipoglucemiantes de la exendina-4 se confirmaron en ensayos clínicos.¹⁵ En 2005, la exenatida se convirtió en el primer análogo de incretina aprobado para la diabetes tipo 2.¹⁶⁻¹⁸ Paralelamente, diversas compañías farmacéuticas centraron sus esfuerzos en sintetizar análogos del receptor GLP-1 para el tratamiento de la diabetes tipo 2, prolongando la vida media del GLP-1 mediante modificaciones aminoacídicas y resistencia a la dipeptidil peptidasa-4 in vivo.¹⁹,²⁰
PUNTOS CLAVE
Agonistas del receptor GLP-1
- Los agonistas del receptor del péptido similar al glucagón-1 (GLP-1) actúan mediante la potenciación de la secreción de insulina mediada por glucosa, efecto que se ve ampliado por los agonistas dobles o triples del receptor GLP-1 y del receptor del péptido insulinotrópico dependiente de glucosa (GIP).
- Los agonistas del receptor GLP-1 reducen indirectamente los niveles de glucosa en sangre al disminuir el vaciamiento gástrico, inhibir la secreción de glucagón y favorecer un microbioma intestinal beneficioso.
- Los agonistas del receptor GLP-1 y del receptor GIP ejercen efectos directos sobre los núcleos hipotalámicos que potencian la saciedad y promueven la pérdida de peso.
- Ensayos aleatorizados y controlados a gran escala han demostrado que los agonistas del receptor GLP-1 reducen el riesgo cardiovascular y la progresión hacia la insuficiencia renal en individuos de alto riesgo y en aquellos con diabetes tipo 2.
- Los eventos adversos y efectos secundarios asociados con los agonistas del receptor GLP-1 son predominantemente gastrointestinales, aunque también incluyen pérdida de masa muscular y ósea.
El péptido insulinotrópico dependiente de glucosa (GIP) fue la primera incretina aislada.²¹,²² El GIP se sintetiza en las células K intestinales y potencia la liberación de insulina mediada por glucosa. Aunque su administración produce solo cambios modestos en la glucemia de pacientes con diabetes tipo 2, ejerce un efecto pro-sobrevida sobre las células beta de los islotes pancreáticos. Al combinarse con agonistas sintéticos del receptor GLP-1, se observan efectos aditivos tanto sobre los niveles glucémicos como sobre el peso corporal. Además, el GIP muestra efectos modestos de sensibilización insulínica en los adipocitos. En conjunto, estos avances inauguraron una nueva era de terapias basadas en GLP-1 que hoy comprenden agonistas dobles y triples, varios de los cuales han sido aprobados por agencias reguladoras internacionales, con más en fase avanzada de desarrollo para la diabetes tipo 2 y la obesidad (Tabla 1).
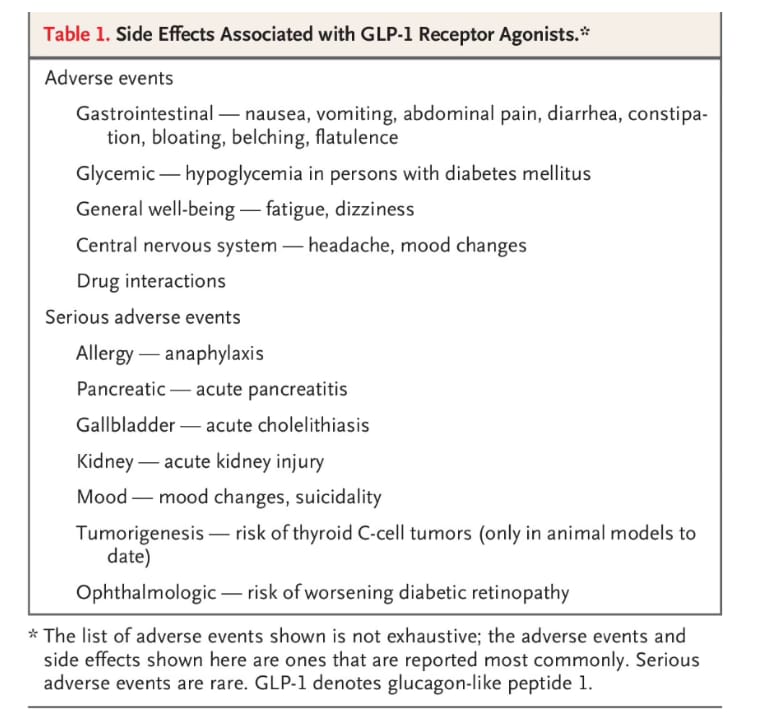
TABLA 1
Efectos secundarios asociados con los agonistas del receptor GLP-1.
Secreción y unión del GLP-1 y el GIP
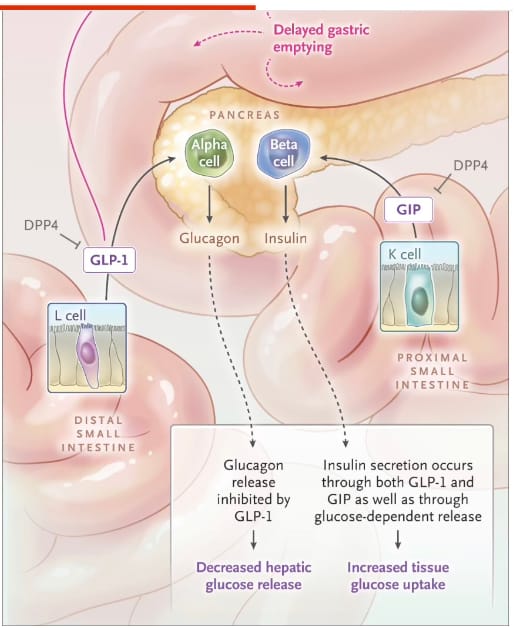
La familia de las incretinas incluye habitualmente el GIP, el GLP-1 y el glucagón.²¹ Todos se producen y secretan por células intestinales específicas en respuesta a las comidas, aunque también se sintetizan en otros tejidos, particularmente en el tronco encefálico. El GLP-1 y el GIP se liberan en respuesta a los niveles de glucosa intestinal, en tanto que la glucosa intravenosa apenas modifica la liberación de incretinas (Figura 1). Estos péptidos intestinales se secretan ante proteínas y lípidos ingeridos cuando la glucemia está elevada, potenciando la liberación de insulina en momentos críticos.²³ Sus vidas medias circulantes son muy breves debido a la degradación intestinal, la actividad enzimática sistémica de la dipeptidil peptidasa-4 y la rápida depuración renal.
FIGURA 1
Efectos fisiológicos de la familia de fármacos incretínicos.
El GLP-1, el GIP y el glucagón poseen receptores propios distribuidos en diversos tejidos del organismo. Dado que su principal mecanismo de acción consiste en estimular la secreción de insulina de forma dependiente de glucosa, las células beta de los islotes pancreáticos presentan la mayor densidad de receptores para estos péptidos.²¹ El GLP-1 se activa al unirse a un receptor acoplado a proteínas G, lo que desencadena la liberación intracelular de monofosfato de adenosina cíclico (cAMP) y la activación de la adenilil ciclasa.²⁴ Este proceso impulsa la captación de Ca²⁺ a través de canales de calcio dependientes de voltaje y la liberación de Ca²⁺ desde depósitos intracelulares, mediada por la activación de Epac2 (proteína de intercambio directamente activada por cAMP 2) en la célula beta. El GIP se une a su receptor acoplado a proteínas G y activa vías idénticas, aunque con mayor dependencia de los canales K⁺ ATP que el GLP-1 en las células insulares.²¹,²⁴ Este complejo entramado de vías e interacciones ha ofrecido dianas terapéuticas accesibles para el control tanto de la hiperglucemia como del exceso ponderal.
Propiedades hipoglucemiantes de los agonistas del receptor GLP-1 y de otras incretinas
El GLP-1 y el GIP promueven directamente la secreción de insulina, inhiben el glucagón y estimulan mecanismos prosurvival y proliferativos de las células beta para preservar la masa insular.²¹,²⁴ El GLP-1, además, ralentiza el vaciamiento gástrico y reduce la motilidad gástrica, contribuyendo así a disminuir los niveles plasmáticos de glucosa. Existen indicios de que los agonistas del receptor GLP-1 podrían modular el microbioma intestinal y mejorar la tolerancia glucídica, aunque se requieren investigaciones adicionales.²⁵ Estos agonistas ejercen efectos mínimos sobre la sensibilidad insulínica en músculo o tejido adiposo, pero generan efectos indirectos sobre la tolerancia glucídica mediante modificaciones en el metabolismo lipídico. Por su parte, el GIP activa AKT (proteína cinasa B), lo que favorece la translocación del transportador de glucosa 4 a la membrana y potencia la captación de glucosa en los adipocitos.²⁶ La secreción de GIP promueve el almacenamiento lipídico, reduciendo los ácidos grasos libres circulantes al incrementar la lipogénesis de novo y estimular la lipasa lipoproteica de los adipocitos.²⁷,²⁸ Estas propiedades potencian la eficacia de la terapia dual con agonistas de los receptores GLP-1 y GIP.
A diferencia del GIP y el GLP-1, el glucagón, hormona contrarreguladora que eleva la glucemia mediante glucogenólisis y gluconeogénesis hepáticas, también aumenta la saciedad gracias a su acción directa en el hipotálamo ventromedial.²⁶ Es notable que el glucagón o sus agonistas, que actúan a través del receptor del glucagón, constituyan adyuvantes prometedores en enfoques combinatorios fijos, particularmente porque reducen la infiltración grasa intrahepática y favorecen la lipólisis. En conjunto, los agonistas del receptor GLP-1, con o sin agonistas del GIP, ejercen efectos profundos sobre la dinámica glucémica mediante estimulación directa de la secreción de insulina y acciones indirectas sobre el metabolismo lipídico, el vaciamiento gástrico y la motilidad intestinal.
Agonistas del receptor GLP-1 y el sistema nervioso central
La regulación de los centros hipotalámicos implicados en el control glucémico y el mantenimiento del peso corporal constituye una característica distintiva de los agonistas del receptor GLP-1. Estos receptores se hallan abundantemente expresados en el núcleo arqueado —que contiene neuronas de proteína relacionada con agutí y neuropéptido Y— y en otras regiones hipotalámicas donde también se produce GLP-1, aunque su síntesis principal ocurre en el tronco encefálico. Los receptores de las incretinas controlan el peso corporal y la ingesta alimentaria de manera independiente del control glucémico. La inyección intracerebroventricular de GLP-1 en el núcleo paraventricular induce saciedad; asimismo, dado que los núcleos de pro-opiomelanocortina expresan receptores GLP-1, se genera un efecto anorexígeno.²⁹ El núcleo arqueado (pero no el paraventricular), rico en receptores GLP-1, regula la glucemia al modular la producción hepática de glucosa. Además, el GLP-1 modifica la utilización de sustratos en ambos núcleos, favoreciendo la oxidación lipídica y reduciendo el cociente de intercambio respiratorio.³⁰
Efecto sobre los niveles de hemoglobina glucosilada
Los ensayos aleatorizados y controlados con placebo de los agonistas del receptor GLP-1 han proporcionado evidencia contundente que respalda su empleo y han anticipado una auténtica revolución en el manejo de la diabetes tipo 2. Tras los ensayos de registro de fase 3 de la exenatida subcutánea administrada dos veces al día, el compuesto de acción prolongada se evaluó en el ensayo DURATION-1 (Efectos de la exenatida de liberación prolongada sobre el control glucémico y la seguridad en sujetos con diabetes mellitus tipo 2), un estudio aleatorizado de fases 1 y 2 con una fase controlada de 30 semanas en la que pacientes con diabetes tipo 2 bajo tratamiento hipoglucemiante (metformina o sulfonilureas) recibieron exenatida de acción prolongada (2 mg una vez por semana) o exenatida de acción corta (10 μg dos veces al día).¹⁹,³¹ Los niveles de hemoglobina glucosilada se redujeron entre un 1,5 % y un 1,9 %, con mayor efecto en la formulación de acción prolongada. Ensayos posteriores con liraglutida confirmaron que los agonistas del receptor GLP-1 de acción prolongada ejercen efectos hipoglucemiantes más intensos y sostenidos que la terapia convencional y superan a la exenatida.³²,³³ El ensayo SUSTAIN 3 de 56 semanas demostró que 1 mg de semaglutida semanal reducía los niveles de hemoglobina glucosilada de forma significativamente superior a 2 mg de exenatida de liberación prolongada semanal.³⁴ En el ensayo PIONEER 2, la semaglutida oral resultó superior a la empagliflozina (inhibidor de SGLT2) en la reducción de la hemoglobina glucosilada.³⁵ Otros ensayos de mayor tamaño corroboraron la superioridad de los agonistas de acción prolongada sobre otras terapias de segunda línea distintas de la metformina en la diabetes tipo 2.³⁶
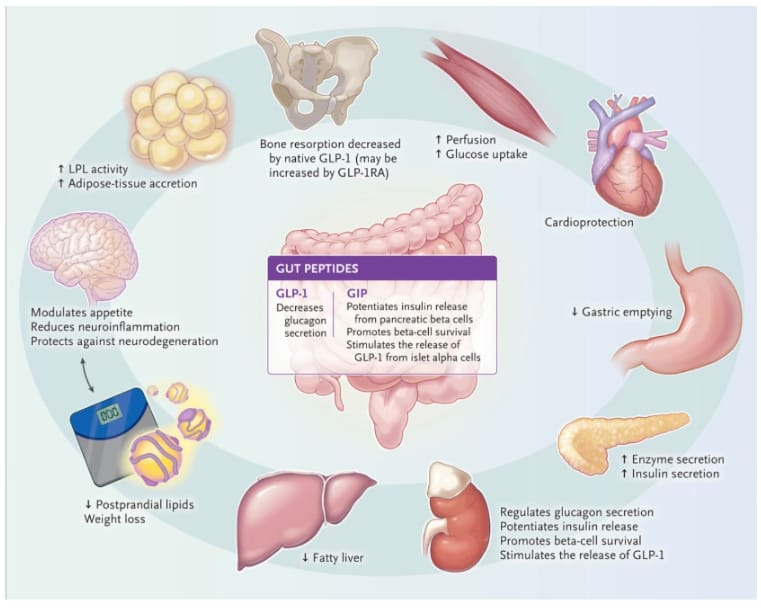
La tirzepatida fue el primer agonista dual de los receptores GLP-1 y GIP aprobado para la diabetes tipo 2, sobre la base del ensayo SURPASS-1 (Tirzepatida [LY3298176] en participantes con diabetes tipo 2 no controlada únicamente con dieta y ejercicio), estudio aleatorizado y controlado con placebo que evaluó tirzepatida (dosis semanales de 5 mg, 10 mg o 15 mg) asociada a metformina (Figura 2). La tirzepatida redujo la hemoglobina glucosilada hasta en 2 puntos porcentuales y superó al placebo en todos los niveles de dosis.³⁷ A las 40 semanas, casi el 90 % de los participantes alcanzaron niveles inferiores al 7,0 %, cambio asociado a una pérdida de peso sustancial. En el ensayo SURPASS-2, la tirzepatida (5 mg, 10 mg o 15 mg semanales) demostró superioridad frente a la semaglutida (1,0 mg semanal).³⁸ Un metaanálisis reciente de ensayos con tirzepatida (15 mg semanal) reveló reducciones de hemoglobina glucosilada comparables a las de los ensayos SURPASS.³⁵ En dicho análisis, la tirzepatida resultó similar a la semaglutida (2,0 mg semanal) en el mantenimiento de la reducción glucémica.³⁹ Además, las tres dosis de tirzepatida superaron a las insulinas de acción prolongada o ultralarga en el control de la hiperglucemia.
FIGURA 2
Efectos de los agonistas combinados de los receptores GLP-1 y GIP.
Más recientemente, la retatrutida —agonista triple de tercera generación de los receptores GLP-1, GIP y glucagón— exhibió excelentes efectos hipoglucemiantes en un amplio ensayo aleatorizado de fase 2 en pacientes con diabetes tipo 2, superior tanto al placebo como a la dulaglutida.⁴⁰ A raíz del desarrollo de estos nuevos agonistas dobles y triples, han surgido algoritmos innovadores para el uso de los agonistas del receptor GLP-1. En particular, su aplicación para prevenir la progresión de prediabetes a diabetes —que afecta a aproximadamente uno de cada tres individuos en tres años— resulta ahora factible.⁴¹ Informes preliminares sugieren que estos agonistas podrían revertir la tolerancia glucídica alterada en la diabetes tipo 1 en estadio 2 (definida por autoanticuerpos relacionados con diabetes y disglicemia asintomática).⁴²
Efectos cardíacos y renales
El control estricto de la glucemia en pacientes con diabetes tipo 2 se asocia con reducción de eventos cardiovasculares adversos mayores (MACE) y menor progresión hacia la insuficiencia renal.⁴³,⁴⁴ No es sorprendente, por tanto, que los ensayos demuestren que los agonistas del receptor GLP-1 no solo disminuyen la hemoglobina glucosilada, sino que también mejoran los resultados cardíacos y renales.⁴⁵⁻⁵⁴ Es probable que los mecanismos subyacentes trasciendan la mera mejora glucémica. Así, el GLP-1 mejora el flujo microvascular al potenciar la función endotelial, inducir vasodilatación y reducir la resistencia vascular sistémica. Otros estudios indican que estos agonistas disminuyen la presión arterial de forma directa e indirecta mediante pérdida de peso y atenuación de la actividad simpática en pacientes con diabetes tipo 2.⁴⁵ El ensayo LEADER (Efecto y acción de la liraglutida en la diabetes: evaluación de los resultados cardiovasculares) demostró tanto la no inferioridad como la superioridad de la liraglutida frente al placebo en cuanto a MACE.⁴⁶ Dos ensayos pivotales con semaglutida —SUSTAIN 6 y PIONEER 6— incluyeron pacientes con diabetes tipo 2 y alto riesgo de complicaciones ateroscleróticas.⁴⁷,⁴⁸ El SUSTAIN 6 reclutó 3927 pacientes, el 83 % de los cuales presentaba enfermedad cardiovascular establecida, enfermedad renal crónica (ERC) o ambas; mostró una reducción del 26 % en el riesgo de MACE (muerte cardiovascular, infarto de miocardio no fatal o ictus no fatal) con semaglutida parenteral semanal.
En PIONEER 6, la semaglutida oral fue no inferior al placebo, aunque sin alcanzar superioridad. En otro ensayo en personas con obesidad y alto riesgo cardiovascular, la semaglutida (2,4 mg semanal) resultó superior al placebo en un criterio compuesto de muerte cardiovascular, infarto de miocardio no fatal o ictus no fatal.⁴⁹ Recientemente, el ensayo SOUL (casi 10 000 pacientes con diabetes tipo 2) demostró que la semaglutida oral (hasta 14 mg diarios) reducía el riesgo de eventos cardiovasculares en un 14 %.⁵⁰
Otro estudio mostró que la tirzepatida reducía la mortalidad en un criterio compuesto de pacientes con insuficiencia cardíaca congestiva.⁵¹ La duración media de los principales ensayos de intervención cardiovascular con GLP-1 fue de aproximadamente tres años; por consiguiente, se requieren estudios de mayor duración.Los ensayos integrados en los estudios cardiovasculares y otros independientes han evidenciado que la progresión de la ERC se retrasa o previene en pacientes con diabetes tipo 2. La progresión se retrasó en promedio unos tres años y, en algunos casos, se evitó por completo. Los efectos renoprotectores de liraglutida, dulaglutida y semaglutida son directos e indirectos y, en parte, independientes de la mejora glucémica.
Las acciones directas incluyen mejoría de la función endotelial, cambios favorables en el intercambio tubular de solutos, atenuación del sistema renina-angiotensina y reducción de la presión arterial, lo que disminuye la prevalencia de ERC.⁵²,⁵³ En LEADER, la liraglutida se asoció con menor macroalbuminuria y menor incidencia y prevalencia de nefropatía diabética, aunque no difirió del placebo en terapia de reemplazo renal continua ni en duplicación de creatinina sérica.⁵⁵ Resultados similares se observaron con dulaglutida en el análisis exploratorio del ensayo REWIND.⁵⁴ En SUSTAIN 6, la semaglutida redujo un 36 % la nefropatía nueva o empeorada y casi un 50 % la macroalbuminuria, sin diferencias significativas en terapia de reemplazo renal.⁴⁷ Un metaanálisis de estos tres ensayos y otros (incluido SELECT, en personas sin diabetes con obesidad y riesgo cardiovascular) mostró una reducción significativa del 18 % en un criterio renal compuesto que incluía insuficiencia renal.⁴⁷ En enero de 2025, la semaglutida recibió aprobación de la FDA para reducir el riesgo de enfermedad renal en pacientes con diabetes tipo 2.
Agonistas del receptor GLP-1 y pérdida de peso
Los primeros ensayos de fase 3 con exenatida ya reportaron pérdida de peso modesta.¹⁶⁻¹⁸ Varios investigadores observaron que los pacientes no solo mejoraban su control glucémico, sino que perdían peso, lo que impulsó ensayos específicos de mayor escala centrados en la pérdida ponderal.⁴⁷ Los resultados fueron impresionantes y, junto con el desarrollo de análogos combinados, consolidaron la concepción de la obesidad como enfermedad. Inicialmente, cinco ensayos aleatorizados, doble ciego y controlados con placebo evaluaron liraglutida —los estudios SCALE—, que reclutaron a más de 5000 participantes, algunos con diabetes tipo 2 y otros con obesidad sin diabetes.⁵⁶ Se obtuvo una pérdida media de peso corporal del 5 % con liraglutida.
En 2014, la liraglutida se convirtió en el primer agonista del receptor GLP-1 aprobado para el manejo de la obesidad.De forma análoga, los ensayos STEP (Efecto del tratamiento con semaglutida en personas con obesidad) reclutaron a más de 5000 participantes con obesidad.⁵⁷ Se asignaron aleatoriamente a semaglutida subcutánea (2,4 mg semanal) o placebo durante 68 semanas, junto con intervención en el estilo de vida. En STEP 1, la reducción media de peso fue del 14,9 % con semaglutida frente al 2,4 % con placebo.⁵⁸ Sobre esta base, la semaglutida se aprobó para obesidad en 2021. En STEP 4 se observó rebote ponderal clínicamente significativo tras la suspensión.⁵⁹ La semaglutida (2,4 mg semanal) atenuó además factores metabólicos asociados con enfermedad hepática, en particular fibrosis hepática en pacientes obesos.⁶⁰La tirzepatida recibió aprobación para pérdida de peso en noviembre de 2023, con dosis inicial de 2,5 mg semanal y escalada hasta 15 mg.⁶¹ La aprobación se basó en SURMOUNT-1, ensayo de fase 3 que trató a 2539 adultos sin diabetes con tirzepatida durante 72 semanas (escalada cada 4 semanas hasta 15 mg).⁶¹ Se lograron pérdidas de peso del 15-21 % frente al 3 % con placebo.
La tirzepatida resultó más eficaz que la semaglutida, con diferencias de 5,27 a 9,57 kg.⁶² La terapia con tirzepatida indujo además resolución clínicamente significativa de la enfermedad hepática por disfunción metabólica (anteriormente esteatohepatitis no alcohólica).⁶³ La retatrutida, agonista triple de tercera generación, alcanzó pérdidas de peso cercanas al 25 %, significativamente superiores a las de dulaglutida en dosis >4 mg semanales.⁵² Asimismo, produjo resolución significativa de la enfermedad hepática por disfunción metabólica.⁶⁴
En síntesis, el tratamiento con agonistas del receptor GLP-1 resulta altamente eficaz en la obesidad, si bien con matices. Se requiere terapia de mantenimiento para prevenir el rebote ponderal, aunque aún se desconoce cuál y durante cuánto tiempo. Además, la pérdida de peso se acompaña de reducción de masa magra que puede tener repercusiones a corto y largo plazo sobre músculo y hueso.
Eventos adversos
Los eventos adversos están bien caracterizados y no son infrecuentes con los análogos de incretinas (Tabla 1). Los efectos gastrointestinales son los más comunes y se observan en prácticamente todos los ensayos durante la escalada de dosis: náuseas, diarrea, estreñimiento y vómitos, principalmente en las primeras 8 semanas.
Dado que estos agonistas ralentizan la motilidad gástrica e intestinal para reducir la absorción de glucosa, tales efectos resultan previsibles. Entre los eventos graves, el contenido gástrico retenido podría teóricamente aumentar el riesgo de aspiración pulmonar, especialmente perioperatoria.⁶⁵ Las tasas de abandono en los ensayos oscilan entre el 4 % y el 8 %, principalmente por efectos gastrointestinales, aunque la duración suele ser de un año o menos. La prevalencia de enfermedad vesicular es mayor con estos agonistas que con placebo. Un metaanálisis de 76 ensayos y más de 100 000 participantes mostró un riesgo 1,5 veces superior de enfermedad vesicular y biliar, especialmente con dosis altas y tratamientos prolongados.⁶⁶ La hipoglucemia es frecuente cuando se combinan con otros hipoglucemiantes, pero no cuando se emplean solos, según un estudio reciente del Departamento de Veteranos en U.S.A.⁶⁷
La pancreatitis se ha notificado de forma anecdótica y rara, posiblemente relacionada con colecistitis; no obstante, ensayos aleatorizados y controlados a largo plazo no muestran diferencias clínicas respecto al placebo. En SURMOUNT-1 se registraron cuatro casos (uno por grupo de dosis y placebo). Un metaanálisis basado en registros electrónicos de 16 millones de personas encontró mayor número de casos con liraglutida y semaglutida frente a naltrexona-bupropión.⁶⁸
No existe evidencia de aumento en neoplasias, cáncer o mortalidad asociada. De hecho, la reducción de peso podría disminuir el riesgo de ciertos cánceres relacionados con la obesidad.
La pérdida de masa magra es un efecto secundario consistente derivado de la pérdida de peso sostenida, incluida la inducida por estos agonistas.⁶⁹ Los datos sobre consecuencias a largo plazo, especialmente en función muscular y ósea, son limitados. Un estudio reciente reportó una pérdida del 1 % de densidad mineral ósea en fémur y columna tras 52 semanas de liraglutida,⁷⁰ atribuible probablemente a mayor resorción ósea, observada también con semaglutida.⁷¹ Se requieren estudios prolongados para evaluar el riesgo de fractura.
Determinación del uso apropiado de los agonistas del receptor GLP-1Los ensayos con agonistas del receptor GLP-1 para control glucémico y pérdida de peso han sido extraordinariamente exitosos. Ello ha motivado propuestas de empleo temprano —en monoterapia, combinación o como agentes duales— como estrategia de primera línea. El uso tradicional de metformina en monoterapia en diabetes tipo 2 podría cuestionarse, aunque el costo sigue siendo un factor relevante. Ante la evidencia de protección renal y cardiovascular de estudios de fase 3 recientes, podría considerarse el inicio con un agonista del receptor GLP-1, un agonista dual como tirzepatida o la combinación de un inhibidor de SGLT2 con un agonista GLP-1. La notable eficacia en pérdida de peso es ampliamente reconocida. Sin embargo, las preguntas sobre quién debe recibir estos agentes y durante cuánto tiempo siguen evolucionando.⁷² De hecho, su uso ha generado ya escasez, dada la magnitud de la reducción de peso corporal observada.⁷³
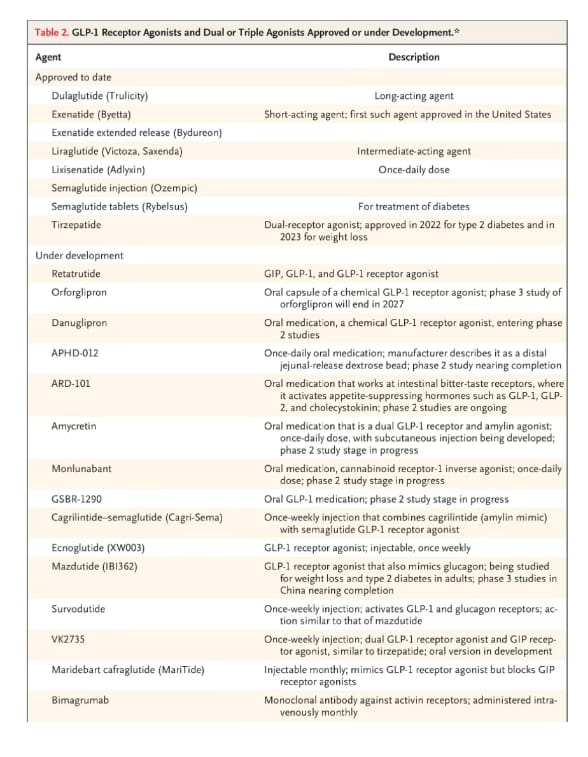
La Tabla 2 enumera los agonistas del receptor GLP-1 actualmente aprobados o en desarrollo.
Aunque este amplio abanico terapéutico genera optimismo acerca de una terapia mejorada para obesidad y diabetes tipo 2, persiste incertidumbre sobre sus beneficios y perfiles de riesgo a largo plazo. Los eventos adversos gastrointestinales observados en ensayos y en práctica clínica suscitan preocupación por la adherencia prolongada y el rebote de ganancia de peso tras la discontinuación.⁷⁴ Tales cuestiones plantean interrogantes adicionales: si estos agentes deben emplearse indefinidamente o de forma episódica, si la microdosificación o la administración menos frecuente serían eficaces, y cómo resolver los aspectos legales y médicos de la preparación magistral para mejorar la asequibilidad sin comprometer la eficacia.
Agonistas del receptor GLP-1 y agonistas duales o triples aprobados o en desarrollo.Agonistas del receptor GLP-1 y equidad en salud
Las poblaciones subrepresentadas suelen excluirse de los ensayos clínicos por diversas razones; por consiguiente, las generalizaciones sobre la eficacia de cualquier fármaco o intervención deben matizarse. Esta limitación resulta especialmente relevante en diabetes tipo 2 y obesidad, donde las personas hispanas y negras constituyen una proporción significativa de los afectados. Aunque el reclutamiento de minorías ha mejorado ligeramente en la última década, las poblaciones de los ensayos rara vez reflejan a las realmente afectadas. Un subestudio de SURPASS-1 mostró respuestas similares en participantes hispanos y no hispanos blancos en cuanto a pérdida de peso y control glucémico.⁷⁶ No obstante, pocos estudios han analizado específicamente la eficacia en poblaciones minoritarias o han incluido suficientes participantes negros o hispanos para extraer conclusiones clínicamente robustas. Esta preocupación se agrava por el elevado costo de los nuevos agonistas. A medida que se acumule evidencia sobre seguridad y eficacia a largo plazo, serán necesarios ajustes de precios y estrategias de distribución equitativa hacia las poblaciones subrepresentadas.
Conclusiones
Los datos clínicos acumulados sitúan a los agentes basados en incretinas en la cúspide del arsenal terapéutico para personas con diabetes tipo 2 u obesidad (o ambas). El desarrollo de nuevos agonistas duales y triples del receptor GLP-1 anticipa la aprobación de fármacos aún más eficaces tras rigurosos ensayos de fase 2 y 3.⁷⁵,⁷⁶ La sólida evidencia de grandes ensayos de fase 3 y numerosos metaanálisis respalda su papel en la estabilización glucémica y en la inducción de pérdidas de peso clínicamente relevantes.⁴⁷,⁷⁷ Asimismo, sus efectos protectores a largo plazo sobre outcomes cardiovasculares y renales son notables. Aunque las señales de seguridad son tranquilizadoras, se requieren estudios de mayor duración, con especial atención al rebote ponderal y a los cambios en masa muscular y ósea. La equidad en salud tanto en los ensayos como en el acceso al mercado es esencial para incluir de manera más amplia a quienes más necesitan estos fármacos. Además, los agonistas del receptor GLP-1 muestran promesa en el abordaje de otros trastornos, como enfermedades neurodegenerativas, enfermedad hepática metabólica, insuficiencia cardíaca y cáncer. El futuro se presenta prometedor mientras estos agonistas del receptor GLP-1 ingresan en su segunda mitad de siglo de investigación.
REFERENCIAS
1.World Health Organization. Global report on diabetes. 2016 (https://iris.who.int/server/api/core/bitstreams/d2997184-51c3-4b0b-aa2c-0cc840424b6c/content).
Go to CitationGoogle Scholar
2.Jastreboff AM, Kushner RF. New frontiers in obesity treatment: GLP-1 and nascent nutrient-stimulated hormone-based therapeutics. Annu Rev Med 2023;74:125-139.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
3.Rosenfeld L. Insulin: discovery and controversy. Clin Chem 2002;48:2270-2288.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
4.Friedman JM. The discovery and development of GLP-1 based drugs that have revolutionized the treatment of obesity. Proc Natl Acad Sci U S A 2024;121(39):e2415550121-e2415550121.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
5.Lund PK, Goodman RH, Dee PC, Habener JF. Pancreatic preproglucagon cDNA contains two glucagon-related coding sequences arranged in tandem. Proc Natl Acad Sci U S A 1982;79:345-349.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
6.Holst JJ. Gut glucagon, enteroglucagon, gut glucagonlike immunoreactivity, glicentin — current status. Gastroenterology 1983;84:1602-1613.
Go to CitationCrossrefPubMedGoogle Scholar
7.Nathan DM, Schreiber E, Fogel H, Mojsov S, Habener JF. Insulinotropic action of glucagonlike peptide-I-(7-37) in diabetic and nondiabetic subjects. Diabetes Care 1992;15:270-276.
Go to CitationCrossrefPubMedGoogle Scholar
8.Mojsov S, Weir GC, Habener JF. Insulinotropin: glucagon-like peptide I (7-37) co-encoded in the glucagon gene is a potent stimulator of insulin release in the perfused rat pancreas. J Clin Invest1987;79:616-619.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
9.Holst JJ, Orskov C, Nielsen OV, Schwartz TW. Truncated glucagon-like peptide I, an insulin-releasing hormone from the distal gut. FEBS Lett 1987;211:169-174.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
10.Drucker DJ, Philippe J, Mojsov S, Chick WL, Habener JF. Glucagon-like peptide I stimulates insulin gene expression and increases cyclic AMP levels in a rat islet cell line. Proc Natl Acad Sci U S A 1987;84:3434-3438.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
11.Kreymann B, Williams G, Ghatei MA, Bloom SR. Glucagon-like peptide-1 7-36: a physiological incretin in man. Lancet 1987;2:1300-1304.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
12.Eng J. Exendin peptides. Mt Sinai J Med 1992;59:147-149. PubMedWeb of ScienceGoogle Scholar
13.Edwards CM, Todd JF, Mahmoudi M, et al. Glucagon-like peptide 1 has a physiological role in the control of postprandial glucose in humans: studies with the antagonist exendin 9-39. Diabetes1999;48:86-93.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
14.Nauck MA, Kleine N, Orskov C, Holst JJ, Willms B, Creutzfeldt W. Normalization of fasting hyperglycaemia by exogenous glucagon-like peptide 1 (7-36 amide) in type 2 (non-insulin-dependent) diabetic patients. Diabetologia 1993;36:741-744.
Go to CitationCrossrefPubMedGoogle Scholar
15.Gutniak M, Orskov C, Holst JJ, Ahrén B, Efendic S. Antidiabetogenic effect of glucagon-like peptide-1 (7-36)amide in normal subjects and patients with diabetes mellitus. N Engl J Med 1992;326:1316-1322.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
16.DeFronzo RA, Ratner RE, Han J, Kim DD, Fineman MS, Baron AD. Effects of exenatide (exendin-4) on glycemic control and weight over 30 weeks in metformin-treated patients with type 2 diabetes. Diabetes Care 2005;28:1092-1100. CrossrefPubMedWeb of ScienceGoogle Scholar
17.Buse JB, Henry RR, Han J, et al. Effects of exenatide (exendin-4) on glycemic control over 30 weeks in sulfonylurea-treated patients with type 2 diabetes. Diabetes Care 2004;27:2628-2635. CrossrefPubMedWeb of ScienceGoogle Scholar
18.Kendall DM, Riddle MC, Rosenstock J, et al. Effects of exenatide (exendin-4) on glycemic control over 30 weeks in patients with type 2 diabetes treated with metformin and a sulfonylurea. Diabetes Care2005;28:1083-1091. CrossrefPubMedWeb of ScienceGoogle Scholar
19.Drucker DJ, Buse JB, Taylor K, et al. Exenatide once weekly versus twice daily for the treatment of type 2 diabetes: a randomised, open-label, non-inferiority study. Lancet 2008;372:1240-1250. CrossrefPubMedWeb of ScienceGoogle Scholar
20.Lau J, Bloch P, Schäffer L, et al. Discovery of the once-weekly glucagon-like peptide-1 (GLP-1) analogue semaglutide. J Med Chem 2015;58:7370-7380.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
21.Nauck MA, Müller TD. Incretin hormones and type 2 diabetes. Diabetologia 2023;66:1780-1795. CrossrefPubMedWeb of ScienceGoogle Scholar
22.McIntosh CH, Widenmaier S, Kim S-J. Glucose-dependent insulinotropic polypeptide signaling in pancreatic β-cells and adipocytes. J Diabetes Investig 2012;3:96-106.
Go to CitationCrossrefPubMedGoogle Scholar
23.Rayas M, Pezzica S, Honka H, et al. GLP-1 enhances β-cell response to protein ingestion and bariatric surgery amplifies it. Obesity (Silver Spring) 2025;33:104-115.
Go to CitationCrossrefPubMedGoogle Scholar
24.McLean BA, Wong CK, Campbell JE, Hodson DJ, Trapp S, Drucker DJ. Revisiting the complexity of GLP-1 action from sites of synthesis to receptor activation. Endocr Rev 2021;42:101-132. CrossrefPubMedWeb of ScienceGoogle Scholar
25.Barakat GM, Ramadan W, Assi G, Khoury NBE. Satiety: a gut-brain-relationship. J Physiol Sci 2024;74:11-11.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
26.Sekar R, Wang L, Chow BKC. Central control of feeding behavior by the secretin, PACAP, and glucagon family of peptides. Front Endocrinol (Lausanne) 2017;8:18-18. CrossrefPubMedWeb of ScienceGoogle Scholar
27.Kagdi S, Lyons SA, Beaudry JL. The interplay of glucose-dependent insulinotropic polypeptide in adipose tissue. J Endocrinol 2024;261(3):e230361-e230361.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
28.Szalowska E, Meijer K, Kloosterhuis N, Razaee F, Priebe M, Vonk RJ. Sub-chronic administration of stable GIP analog in mice decreases serum LPL activity and body weight. Peptides 2011;32:938-945.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
29.Kabahizi A, Wallace B, Lieu L, et al. Glucagon-like peptide-1 (GLP-1) signalling in the brain: from neural circuits and metabolism to therapeutics. Br J Pharmacol 2022;179:600-624.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
30.Abtahi S, Howell E, Salvucci JT, Bastacky JMR, Dunn DP, Currie PJ. Exendin-4 antagonizes the metabolic action of acylated ghrelinergic signaling in the hypothalamic paraventricular nucleus. Gen Comp Endocrinol 2019;270:75-81.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
31.Buse JB, Drucker DJ, Taylor KL, et al. DURATION-1: exenatide once weekly produces sustained glycemic control and weight loss over 52 weeks. Diabetes Care 2010;33:1255-1261.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
32.Buse JB, Rosenstock J, Sesti G, et al. Liraglutide once a day versus exenatide twice a day for type 2 diabetes: a 26-week randomised, parallel-group, multinational, open-label trial (LEAD-6). Lancet2009;374:39-47.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
33.Blevins T, Pullman J, Malloy J, et al. DURATION-5: exenatide once weekly resulted in greater improvements in glycemic control compared with exenatide twice daily in patients with type 2 diabetes. J Clin Endocrinol Metab 2011;96:1301-1310.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
34.Ahmann AJ, Capehorn M, Charpentier G, et al. Efficacy and safety of once-weekly semaglutide versus exenatide ER in subjects with type 2 diabetes (SUSTAIN 3): a 56-week, open-label, randomized clinical trial. Diabetes Care 2018;41:258-266.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
35.Rodbard HW, Rosenstock J, Canani LH, et al. Oral semaglutide versus empagliflozin in patients with type 2 diabetes uncontrolled on metformin: the PIONEER 2 trial. Diabetes Care 2019;42:2272-2281. CrossrefPubMedWeb of ScienceGoogle Scholar
36.Xie Y, Choi T, Al-Aly Z. Author correction: mapping the effectiveness and risks of GLP-1 receptor agonists. Nat Med 2025;31:1038-1038.
Go to CitationCrossrefPubMedGoogle Scholar
37.Rosenstock J, Wysham C, Frías JP, et al. Efficacy and safety of a novel dual GIP and GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1): a double-blind, randomised, phase 3 trial. Lancet 2021;398:143-155.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
38.Frías JP, Davies MJ, Rosenstock J, et al. Tirzepatide versus semaglutide once weekly in patients with type 2 diabetes. N Engl J Med 2021;385:503-515.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
39.Yang X-Y, Yin S, Yu Y-F, et al. Is tirzepatide 15 mg the preferred treatment strategy for type 2 diabetes? A meta-analysis and trial-sequence-analysis. Eur Rev Med Pharmacol Sci 2023;27:7164-7179.
Go to CitationPubMedGoogle Scholar
40.Rosenstock J, Frias J, Jastreboff AM, et al. Retatrutide, a GIP, GLP-1 and glucagon receptor agonist, for people with type 2 diabetes: a randomised, double-blind, placebo and active-controlled, parallel-group, phase 2 trial conducted in the USA. Lancet 2023;402:529-544.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
41.Jastreboff AM, le Roux CW, Stefanski A, et al. Tirzepatide for obesity treatment and diabetes prevention. N Engl J Med 2025;392:958-971.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
42.Edwards K, Li X, Lingvay I. Clinical and safety outcomes with GLP-1 receptor agonists and SGLT2 inhibitors in type 1 diabetes: a real-world study. J Clin Endocrinol Metab 2023;108:920-930.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
43.Reaven PD, Emanuele NV, Wiitala WL, et al. Intensive glucose control in patients with type 2 diabetes — 15-year follow-up. N Engl J Med 2019;380:2215-2224.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
44.Ruospo M, Saglimbene VM, Palmer SC, et al. Glucose targets for preventing diabetic kidney disease and its progression. Cochrane Database Syst Rev 2017;6:CD010137-CD010137.
Go to CitationPubMedGoogle Scholar
45.Helmstädter J, Frenis K, Filippou K, et al. Endothelial GLP-1 (glucagon-like peptide-1) receptor mediates cardiovascular protection by liraglutide in mice with experimental arterial hypertension. Arterioscler Thromb Vasc Biol 2020;40:145-158. CrossrefPubMedWeb of ScienceGoogle Scholar
46.Rahman A, Alqaisi S, Saith SE, Alzakhari R, Levy R. The impact of glucagon-like peptide-1 receptor agonist on the cardiovascular outcomes in patients with type 2 diabetes mellitus: a meta-analysis and systematic review. Cardiol Res 2023;14:250-260. CrossrefPubMedWeb of ScienceGoogle Scholar
47.Marso SP, Bain SC, Consoli A, et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2016;375:1834-1844. CrossrefPubMedWeb of ScienceGoogle Scholar
48.Husain M, Birkenfeld AL, Donsmark M, et al. Oral semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2019;381:841-851. CrossrefPubMedWeb of ScienceGoogle Scholar
49.Lincoff AM, Brown-Frandsen K, Colhoun HM, et al. Semaglutide and cardiovascular outcomes in obesity without diabetes. N Engl J Med 2023;389:2221-2232. CrossrefPubMedWeb of ScienceGoogle Scholar
50.McGuire DK, Marx N, Mulvagh SL, et al. Oral semaglutide and cardiovascular outcomes in high risk Type 2 Diabetes. N Engl J Med 2025;392:2001-2012. CrossrefPubMedWeb of ScienceGoogle Scholar
51.Packer M, Zile MR, Kramer CM, et al. Tirzepatide for heart failure with preserved ejection fraction and obesity. N Engl J Med 2025;392:427-437. CrossrefPubMedWeb of ScienceGoogle Scholar
52.Badve SV, Bilal A, Lee MMY, et al. Effects of GLP-1 receptor agonists on kidney and cardiovascular disease outcomes: a meta-analysis of randomised controlled trials. Lancet Diabetes Endocrinol2025;13:15-28. CrossrefPubMedWeb of ScienceGoogle Scholar
53.Lee B, Holstein-Rathlou N-H, Sosnovtseva O, Sørensen CM. Renoprotective effects of GLP-1 receptor agonists and SGLT-2 inhibitors-is hemodynamics the key point? Am J Physiol Cell Physiol2023;325(1):C243-C256. CrossrefPubMedGoogle Scholar
54.Gerstein HC, Colhoun HM, Dagenais GR, et al. Dulaglutide and renal outcomes in type 2 diabetes: an exploratory analysis of the REWIND randomised, placebo-controlled trial. Lancet 2019;394:131-138. CrossrefPubMedWeb of ScienceGoogle Scholar
55.Mann JFE, Ørsted DD, Brown-Frandsen K, et al. Liraglutide and renal outcomes in type 2 diabetes. N Engl J Med 2017;377:839-848.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
56.Davies MJ, Bergenstal R, Bode B, et al. Efficacy of liraglutide for weight loss among patients with type 2 diabetes: the SCALE diabetes randomized clinical trial. JAMA 2015;314:687-699.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
57.Amaro A, Sugimoto D, Wharton S. Efficacy and safety of semaglutide for weight management: evidence from the STEP program. Postgrad Med 2022;134:5-17.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
58.Wilding JPH, Batterham RL, Calanna S, et al. Once-weekly semaglutide in adults with overweight or obesity. N Engl J Med 2021;384:989-1002.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
59.Rubino D, Abrahamsson N, Davies M, et al. Effect of continued weekly subcutaneous semaglutide vs placebo on weight loss maintenance in adults with overweight or obesity: the STEP 4 randomized clinical trial. JAMA 2021;325:1414-1425.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
60.Alkhouri N, Charlton M, Gray M, Noureddin M. The pleiotropic effects of glucagon-like peptide-1 receptor agonists in patients with metabolic dysfunction-associated steatohepatitis: a review for gastroenterologists. Expert Opin Investig Drugs 2025;34:169-195.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
61.Jastreboff AM, Aronne LJ, Ahmad NN, et al. Tirzepatide once weekly for the treatment of obesity. N Engl J Med 2022;387:205-216. CrossrefPubMedWeb of ScienceGoogle Scholar
62.Karagiannis T, Malandris K, Avgerinos I, et al. Subcutaneously administered tirzepatide vs semaglutide for adults with type 2 diabetes: a systematic review and network meta-analysis of randomised controlled trials. Diabetologia 2024;67:1206-1222.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
63.Loomba R, Hartman ML, Lawitz EJ, et al. Tirzepatide for metabolic dysfunction–associated steatohepatitis with liver fibrosis. N Engl J Med 2024;391:299-310.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
64.Sanyal AJ, Kaplan LM, Frias JP, et al. Triple hormone receptor agonist retatrutide for metabolic dysfunction-associated steatotic liver disease: a randomized phase 2a trial. Nat Med 2024;30:2037-2048.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
65.Jalleh RJ, Plummer MP, Marathe CS, et al. Clinical consequences of delayed gastric emptying with GLP-1 receptor agonists and tirzepatide. J Clin Endocrinol Metab 2024;110:1-15.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
66.He L, Wang J, Ping F, et al. Association of glucagon-like peptide-1 receptor agonist use with risk of gallbladder and biliary diseases: a systematic review and meta-analysis of randomized clinical trials. JAMA Intern Med 2022;182:513-519.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
67.Xie Y, Choi T, Al-Aly Z. Mapping the effectiveness and risks of GLP-1 receptor agonists. Nat Med2025;31:951-962.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
68.Hu E-H, Tsai M-L, Lin Y, Chou T-S, Chen T-H. A review and meta-analysis of the safety and efficacy of using glucagon-like peptide-1 receptor agonists. Medicina (Kaunas) 2024;60:357-357.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
69.Rosen CJ, Horowitz MC. Nutrient regulation of bone marrow adipose tissue: skeletal implications of weight loss. Nat Rev Endocrinol 2023;19:626-638.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
70.Jensen SBK, Sørensen V, Sandsdal RM, et al. Bone health after exercise alone, GLP-1 receptor agonist treatment, or combination treatment: a secondary analysis of a randomized clinical trial. JAMA Netw Open 2024;7(6):e2416775-e2416775.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
71.Hansen MS, Wölfel EM, Jeromdesella S, et al. Once-weekly semaglutide versus placebo in adults with increased fracture risk: a randomised, double-blinded, two-centre, phase 2 trial. EClinicalMedicine2024;72:102624-102624.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
72.Madsbad S, Holst JJ. The promise of glucagon-like peptide 1 receptor agonists (GLP-1RA) for the treatment of obesity: a look at phase 2 and 3 pipelines. Expert Opin Investig Drugs 2025;34:197-215.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
73.Gentinetta S, Sottotetti F, Manuelli M, Cena H. Dietary recommendations for the management of gastrointestinal symptoms in patients treated with GLP-1 receptor agonist. Diabetes Metab Syndr Obes2024;17:4817-4824.
Go to CitationCrossrefPubMedGoogle Scholar
74.Moll H, Frey E, Gerber P, et al. GLP-1 receptor agonists for weight reduction in people living with obesity but without diabetes: a living benefit-harm modelling study. EClinicalMedicine 2024;73:102661-102661.
Go to CitationCrossrefPubMedGoogle Scholar
75.Frías JP, Galindo RJ, Wang H, Malik RE, Chivukula KK, Maldonado JM. Tirzepatide in Hispanic/Latino patients with type 2 diabetes: a subgroup analysis of the SURPASS Program. J Clin Endocrinol Metab2024;109:557-568.
Go to CitationCrossrefPubMedWeb of ScienceGoogle Scholar
76.Véniant MM, Lu S-C, Atangan L, et al. A GIPR antagonist conjugated to GLP-1 analogues promotes weight loss with improved metabolic parameters in preclinical and phase 1 settings. Nat Metab2024;6:290-303. CrossrefPubMedWeb of ScienceGoogle Scholar
77.Caruso I, Di Gioia L, Di Molfetta S, et al. Glucometabolic outcomes of GLP-1 receptor agonist-based therapies in patients with type 2 diabetes: a systematic review and network meta-analysis. EClinicalMedicine 2023;64:102181-102181.