Ronald Palacios Castrillo
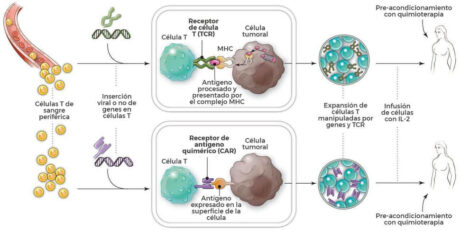
La terapia con células T-CAR es un tipo de inmunoterapia que modifica las células T para que puedan detectar y combatir las células cancerosas. Esta terapia se utiliza cada vez más para tratar a pacientes pediátricos con leucemia linfoblástica aguda de células B y, en casos raros, ciertos tipos de linfoma.
Pero, ¿en qué se diferencia la terapia con células T-CAR para pacientes pediátricos del tratamiento utilizado para pacientes adultos? ¿Y cuáles son los efectos secundarios?
¿Cómo se determina si un paciente pediátrico es un buen candidato para la terapia con células T -CAR?
=> Recibir por Whatsapp las noticias destacadas
Actualmente, contamos con células T-CAR aprobadas por la FDA para tratar a pacientes en recaída y refractarios hasta los 25 años. Estos son pacientes cuyo cáncer ha regresado o cuyo cáncer ha dejado de responder al tratamiento.
Necesitan tener un buen estado funcional y la expresión correcta, como CD19, en la superficie de las células cancerosas. CD19 es un marcador de células B y el objetivo de la terapia con células T -CAR.
A menudo utilizamos la terapia de células T-CAR para lograr que los pacientes con leucemia entren en remisión, de modo que puedan recibir un trasplante de células madre.
¿Puede describir el proceso de la terapia concélulas T – CAR para pacientes pediátricos?
Primero, el paciente recibe un examen exhaustivo que incluye evaluaciones y pruebas de órganos para asegurarse de que esté lo suficientemente sano como para soportar el proceso de recolección, la quimioterapia y la infusión de T-CAR en sí.
Después de eso, los pasos son los siguientes:
- Colección de células
Un cirujano pediátrico colocará un catéter especial llamado catéter de aféresis en el paciente. Esto se hace mientras el niño está bajo anestesia. El mismo día, el paciente se somete a una recolección de células en la que se extraen células T de la sangre del paciente a través del nuevo catéter.
Aparte de algunas pequeñas molestias en el lugar donde se coloca el nuevo catéter, los pacientes pediátricos generalmente toleran muy bien el procedimiento. Dado que el catéter solo se coloca para la recolección, se retira inmediatamente después de que se completa la recolección, generalmente el segundo día. A los pacientes pediátricos se les pone a dormir para colocar el catéter, pero no para retirarlo, por lo que están despiertos mientras les retiran las suturas y les aplican presión en esa área. Naturalmente, no están muy contentos con esto, por lo que, con la ayuda y la experiencia de los especialistas en vida infantil, se habla con los pacientes y se less ayuda a que se sientan cómodos.
Se Trabaja en estrecha colaboración con el equipo de leucemia pediátrica para determinar el mejor momento para la recolección. En algunos casos, los pacientes con leucemia pueden estar tomando esteroides y se trata de evitar la recolección mientras el paciente está tomando corticosteroides (porque disminuyen el número de linfocitos circulantes).
- Fabricación de células
El laboratorio de terapia celular congela las células antes de enviarlas a un laboratorio especializado donde son modificadas genéticamente. Dependiendo del producto, pasan unas tres semanas antes de que sean enviados de regreso al hospital.
- Terapia puente
Cuando se modifican las células T, los pacientes recibirán una pequeña cantidad de quimioterapia para mantener a raya la leucemia. Esto se llama terapia puente.
Si hemos tratado al paciente antes, se conoce bastante bien su historial de tratamiento. Por lo tanto, si un determinado tratamiento los eliminó la última vez o provocó que los recuentos sanguíneos del paciente bajaran extremadamente, esta vez se puede probar algo más suave. Se Trabaja en estrecha colaboración con el equipo de leucemia pediátrica para mantener los recuentos sanguíneos del paciente en un rango seguro mientras recibe quimioterapia.
- Infusión
Una vez que las células modificadas regresan al hospital (e.g. MD Anderson Cancer center), el paciente recibe quimioterapia depleción de linfocitos. Esto significa que eliminará los linfocitos para dejar espacio a las nuevas células CAR-T y permitirles multiplicarse. Luego, las células CAR- T se infunden en la sangre del paciente. Este proceso es rápido, normalmente entre 5 y 30 minutos. Cuando se trata de un procedimiento hospitalario, los pacientes pasarán unas tres semanas en el hospital antes de que sea seguro regresar a casa.
Los pacientes adultos con CAR-T pueden recibir sus infusiones de forma ambulatoria. El objetivo es ofrecer la infusión como procedimiento ambulatorio en el futuro también para pacientes pediátricos.
- Controle los efectos secundarios
Después de la infusión, se controla al paciente para detectar efectos secundarios. Se Realizan varias evaluaciones para ver cómo están funcionando. Una de las evaluaciones es una evaluación neurológica llamada Evaluación Cornell del delirio pediátrico (CAPD). Es una serie de preguntas, que incluyen: «¿El paciente está haciendo movimientos intencionados?» ¿El paciente hace contacto visual? ¿El paciente expresa sus necesidades?’ También se hacen evaluaciones de escritura a mano y, si el paciente es muy pequeño, le pedimos que haga dibujos.
Una vez que los pacientes son dados de alta, generalmente vienen al menos dos veces por semana para seguimiento. Luego también se hacen evaluaciones y se involucra a la familia. Después de todo, ellos conocen mejor al paciente. Las evaluaciones continúan durante ocho semanas después de la infusión.
Una vez que los pacientes reciben la infusión de células T -CAR, se continúa su seguimiento a largo plazo. Si no hay una recaída de la enfermedad, no necesariamente volverán a ver a su médico especializado en leucemia o linfoma. Los pacientes procederán a un trasplante de médula ósea o recibirán atención CAR-T a largo plazo, donde se observan sus células B y se controla su condición.
¿Cuáles son los efectos secundarios de la terapia con células T-CAR en pacientes pediátricos? ¿Cómo los gestionas?
Los dos efectos secundarios más importantes que se observan son el síndrome de liberación de citocinas (RSC) y la neurotoxicidad, también conocida como síndrome de neurotoxicidad asociada a células efectoras inmunitarias (ICANS). El RSC es común y casi siempre ocurre primero. El RSC puede causar síntomas similares a los de la gripe, como fiebre alta y fatiga. Esto se debe a los altos niveles de citocinas producidas por la multiplicación de las células T. Generalmente se empiezan a ver estos efectos secundarios unos tres días después de la infusión, pero también pueden ocurrir más tarde.
La ICANS se identifica en diferentes grados, según la gravedad de los síntomas neurológicos. Los síntomas pueden variar desde una confusión leve, como que el paciente diga cosas que no quiere decir usando sílabas no deseadas, hasta síntomas más graves, como convulsiones. La ICANS puede ocurrir junto con el CRS, pero rara vez es el primer efecto secundario. Los pacientes pueden desarrollar ICANS con CRS o una vez que el CRS se resuelve.
Por lo general, se inicia dándole al paciente un inhibidor de IL-6 como tocilizumab para controlar los síntomas del RSC. Si los síntomas no desaparecen después de dos o tres dosis, o los síntomas se vuelven más graves, usaremos terapias adicionales, como corticoesteroides.
Las evaluaciones son uno de los primeros indicadores de neurotoxicidad. Si un paciente escribe la misma frase dos veces al día, se puede ver un gran cambio en la escritura si comienza a desarrollar neurotoxicidad. Se pueden tratar los efectos secundarios tempranamente sin destruir las células CAR-T que queremos que circulen.
La terapia con células T -CAR se dirige a las células B del paciente, tanto cancerosas como no cancerosas. Esto puede causar un recuento extremadamente bajo de células B, una condición conocida como aplasia de células B. Este es un buen indicador de que un paciente todavía tiene células T -CAR en circulación. Se seguirán controlando las células B de los pacientes después de la infusión. Han habido algunos pacientes que perdieron sus células B 30 días después de la infusión; para otros, ocurre unos meses después del tratamiento. La aplasia de células B no es algo malo desde nuestra perspectiva. Si un paciente lo padece a largo plazo, es casi como si tuviera pequeños luchadores contra el cáncer monitoreando continuamente su cuerpo. Cuando empiezan a recuperar sus células B, preocupa que estén perdiendo sus células CAR-T. Por suerte, podemos vivir sin células B. La aplasia de células B no es ideal, pero es mejor que el cáncer.Se podría infundir inmunoglobulina humana endovenosa cada 21 días para restaurar niveles de anticuerpos en los pacientes.
¿Qué nuevas investigaciones se están realizando para avanzar en el tratamiento de pacientes pediátricos con terapia de células T -CAR?
La terapia con células T-CAR sigue siendo un tratamiento nuevo, que está disponible para pacientes en recaída y refractarios. Se están realizando ensayos clínicos para ver si es beneficioso usarlos como terapia inicial para que los pacientes pediátricos puedan evitar la quimioterapia intensa.
Debido a que estamos aprendiendo cosas nuevas sobre la terapia con células T-CAR, es una opción de tratamiento viable para más pacientes y familias. Si tu hijo lo necesita, busca centros médicos con experiencia como el MD Anderson cancer Center y el St.Jude Children Hospital en New Jersey ,y estará en buenas manos.
Fuente: eju.tv