Antecedentes y objetivos
Los objetivos de este estudio de casos y controles fueron (1) desarrollar una red neuronal convolucional (CNN) tridimensional (3D) automatizada para la detección de adenocarcinoma ductal pancreático (PDA) en exploraciones por tomografía computarizada (TC) de diagnóstico, (2) evaluar su generalización en conjuntos de datos públicos multiinstitucionales, (3) su utilidad como posible herramienta de detección utilizando una cohorte simulada con alta probabilidad previa a la prueba, y (4) su capacidad para detectar cáncer preinvasivo visualmente oculto en TC de prediagnóstico.
Métodos
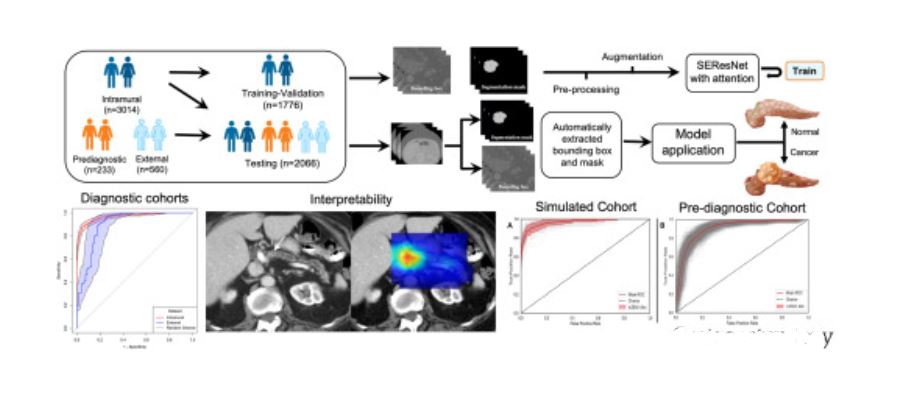
Se entrenó un sistema de clasificación 3D-CNN utilizando cuadros delimitadores generados algorítmicamente y máscaras pancreáticas en un conjunto de datos seleccionados de 696 TC de diagnóstico en fase portal con PDA y 1080 imágenes de control con un páncreas no neoplásico. El modelo se evaluó en (1) un subconjunto de pruebas de resistencia intramuros (409 CT con PDA, 829 controles); (2) una cohorte simulada con una distribución de casos y controles que coincidía con el riesgo de CAP en la diabetes de nueva aparición definida glucémicamente y una puntuación de diabetes enriquecedora de nueva aparición para el cáncer de páncreas ≥3; (3) conjuntos de datos públicos multiinstitucionales (194 TC con CAP, 80 controles) y (4) una cohorte de 100 TC prediagnóstico (es decir, TC adquiridas incidentalmente entre 3 y 36 meses antes del diagnóstico clínico de CAP) sin una masa focal, y 134 controles.
=> Recibir por Whatsapp las noticias destacadas
Resultados
De las TC del subconjunto de pruebas intramuros, 798 (64%) eran de otros hospitales. El modelo clasificó correctamente 360 TC (88 %) con PDA y 783 TC de control (94 %), con una precisión media de 0,92 (IC del 95 %, 0,91–0,94), un área bajo la curva de características operativas del receptor (AUROC) de 0,97 (95 %). % IC, 0,96–0,98), sensibilidad de 0,88 (IC 95 %, 0,85–0,91) y especificidad de 0,95 (IC 95 %, 0,93–0,96). Las áreas de activación en los mapas de calor se superpusieron con el tumor en 350 de 360 TC (97%). El rendimiento fue alto en todos los estadios del tumor (sensibilidad de 0,80, 0,87, 0,95 y 1,0 en los estadios T1 a T4, respectivamente), comparable para tumores hipodensos versus isodensos (sensibilidad: 0,90 versus 0,82), diferentes edades, sexo, espesores de corte de TC y proveedores (todos P > 0,05) y generalizable tanto en la cohorte simulada (precisión, 0,95 [95% 0,94–0,95]; curva AUROC, 0,97 [IC 95%, 0,94–0,99]) como en conjuntos de datos públicos (precisión, 0,86 [IC del 95 %, 0,82–0,90]; curva AUROC, 0,90 [IC del 95 %, 0,86–0,95]). A pesar de estar entrenado exclusivamente en TC de diagnóstico con tumores más grandes, el modelo pudo detectar PDA oculto en TC de prediagnóstico (precisión, 0,84 [IC del 95 %, 0,79–0,88]; curva AUROC, 0,91 [IC del 95 %, 0,86–0,94]; sensibilidad, 0,75 [IC del 95 %, 0,67–0,84] y especificidad, 0,90 [IC del 95 %, 0,85–0,95]) en una mediana de 475 días (rango, 93-1082 días) antes del diagnóstico clínico.
Conclusiones
Este modelo automatizado de inteligencia artificial entrenado en un conjunto de datos grande y diverso muestra una alta precisión y un rendimiento generalizable para la detección de PDA en TC de diagnóstico, así como de PDA visualmente oculto en TC de prediagnóstico. Se justifica la validación prospectiva con biomarcadores sanguíneos para evaluar el potencial de detección temprana del CAP esporádico en individuos de alto riesgo.
El modelo de IA automatizado ayuda en la detección temprana del cáncer de páncreas
31 de enero de 2024
Si se especializa en cáncer de páncreas, sabrá que es muy difícil de diagnosticar: los síntomas clínicos son fáciles de pasar por alto y es posible que no aparezcan hasta las últimas etapas de la enfermedad. Investigadores de la Clínica Mayo financiados por el NCI han creado una herramienta que podría facilitar el diagnóstico temprano en el futuro y se centra en una red neuronal convolucional automatizada.
Lea el artículo completo en Gastroenterología.
La herramienta de los investigadores tiene algunas ventajas clave sobre modelos anteriores. El modelo:
Resiste las pruebas en un conjunto de datos muy grande (es decir, utilizando 1.776 tomografías computarizadas [TC] de pacientes con diversos datos demográficos e imágenes obtenidas con una variedad de configuraciones de máquina).
Identifica cánceres indetectables en tomografías computarizadas de páncreas aparentemente normales hasta 438 días antes del diagnóstico clínico.
Muestra resultados similares tanto en tumores grandes como pequeños.
Ofrece un enfoque totalmente automatizado que requiere poca o ninguna intervención humana.
El autor principal y correspondiente, el Dr. Ajit H. Goenka, dijo: “Sabemos que las TC albergan cánceres ‘visualmente ocultos’; es decir, cánceres que están presentes en la TC, pero que están más allá del alcance de la percepción humana. Al entrenar nuestro modelo con una cantidad tan grande y diversa de datos de TC, podemos distinguir cambios en la textura pancreática que podrían ayudar a identificar el cáncer meses antes que nuestros métodos de atención estándar actuales”.
Un modelo de este tipo podría ser una parte clave del diagnóstico en el futuro. Dijo el Dr. Goenka: «Nuestro modelo podría servir como un segundo ‘par de ojos’, ayudando a los radiólogos y otros especialistas a ver cambios celulares sutiles o pequeños que señalan la presencia o potencial de cáncer de páncreas».